题目内容
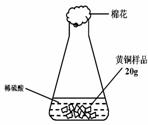
黄铜(铜锌合金)在生产生活中有重要用途.某研究性学习小组的同学,为测定某种品牌中的锌的质量分数是否符合国标的规定(32~38%),设计了如图1所示的实验装置进行检测.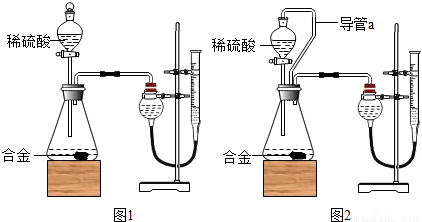
(1)检查气密性并开始实验时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶.经过研讨他们找到了问题的症结,改用图2装置进行,其中导管a的作用是 和 .
(2)若称量的合金质量为10g,充分反应后量取的气体体积为1000mL,通过计算该样品是否合格?(已知氢气的密度为0.089g/L)
(3)另外一个小组的同学用托盘天平称量法也粗略地完成了测定.他们先称取m1g合金置于烧杯(质量为m2g)中,待加入足量稀硫酸(质量为m3g)后不再产生气泡了,称得烧杯和剩余物质总质量为m4g,若(m1+m2+m3)-m4=0.2g,要保证合金样品中的锌完全反应,m1至少为多少克?(写出具体计算过程)
反思:若(2)中的各项质量不变,而采用(3)的方法进行测定是否可行?理由是 .
【答案】分析:(1)根据装置特点及根据压强对溶液的影响分析;
(2)根据生成氢气的体积计算其质量,并计算锌的质量,从而求出合金中锌的质量分数,确定是否合格;
(3)根据氢气的质量和锌的质量分数分析解答;气体的质量<0.1g,用天平无法称量.
解答:解:(1)锌与稀硫酸反应产生的氢气使锥形瓶内气压增大,锥形瓶内的压强大于大气压,导管a使锥形瓶内的气体进入分液漏斗上方,使分液漏斗上方的压强增大,稀硫酸顺利滴下;
故答案为:平衡锥形瓶与分液漏斗内的压强;使稀硫酸顺利滴下;
(2)设样品中锌的质量是X
Zn+H2SO4═ZnSO4+H2↑
65 2
X 1Lⅹ0.089g/L=0.089g
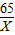 =
=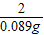
∴X=2.89g
则样品中锌的质量分数是: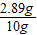 ×100%=28.9%<32%
×100%=28.9%<32%
答:该样品不合格.
(3)设生成0.2g氢气,需要锌的质量是Y
Zn+H2SO4═ZnSO4+H2↑
65 2
Y 0.2g
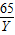 =
=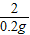
Y=6.5g
m1=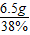 =17.1g
=17.1g
答:m1至少为17.1克
[反思]:若(2)中的各项质量不变,而采用(3)的方法进行测定,该法不可行,因为减少的质量为0.089g,天平能精确到0.1g,故无法用托盘天平称量;
故答案为:不可行,减少的质量为0.089g,无法用托盘天平称量.
点评:本题主要考查了利用方程式的计算及对实验装置的分析,能很好的考查学生应用所学知识分析和解决问题的能力,有一定难度.
(2)根据生成氢气的体积计算其质量,并计算锌的质量,从而求出合金中锌的质量分数,确定是否合格;
(3)根据氢气的质量和锌的质量分数分析解答;气体的质量<0.1g,用天平无法称量.
解答:解:(1)锌与稀硫酸反应产生的氢气使锥形瓶内气压增大,锥形瓶内的压强大于大气压,导管a使锥形瓶内的气体进入分液漏斗上方,使分液漏斗上方的压强增大,稀硫酸顺利滴下;
故答案为:平衡锥形瓶与分液漏斗内的压强;使稀硫酸顺利滴下;
(2)设样品中锌的质量是X
Zn+H2SO4═ZnSO4+H2↑
65 2
X 1Lⅹ0.089g/L=0.089g
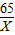 =
=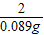
∴X=2.89g
则样品中锌的质量分数是:
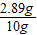 ×100%=28.9%<32%
×100%=28.9%<32%答:该样品不合格.
(3)设生成0.2g氢气,需要锌的质量是Y
Zn+H2SO4═ZnSO4+H2↑
65 2
Y 0.2g
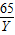 =
=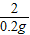
Y=6.5g
m1=
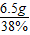 =17.1g
=17.1g答:m1至少为17.1克
[反思]:若(2)中的各项质量不变,而采用(3)的方法进行测定,该法不可行,因为减少的质量为0.089g,天平能精确到0.1g,故无法用托盘天平称量;
故答案为:不可行,减少的质量为0.089g,无法用托盘天平称量.
点评:本题主要考查了利用方程式的计算及对实验装置的分析,能很好的考查学生应用所学知识分析和解决问题的能力,有一定难度.

练习册系列答案
相关题目






 ⑴下列生活用品,主要利用金属具有良好导热性的是:___ ____。
⑴下列生活用品,主要利用金属具有良好导热性的是:___ ____。