题目内容
7. 某纯碱样品中含有少量NaCl,小丽同学取该样品23g全部溶解于150g水中,再逐滴加人160g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示.计算当恰好完全反应时:
某纯碱样品中含有少量NaCl,小丽同学取该样品23g全部溶解于150g水中,再逐滴加人160g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示.计算当恰好完全反应时:(1)产生的二氧化碳的质量是8.8克;
(2)样品中碳酸钠的质量为21.2克;
(3)此时所得到的溶液中氯化钠的质量分数为多少?(写出必要的计算过程,结果保留到0.1% ).
分析 根据已有的知识进行分析解答,据图即可知道生成的二氧化碳的质量,根据二氧化碳的质量求出参加反应的碳酸钠的质量和生成的氯化钠的质量,然后根据溶质质量分数公式计算即可.
解答 解:(1)据图可以看出,生成的二氧化碳的质量为8.8g,故填:8.8;
(2)设碳酸钠的质量为x,生成的氯化钠的质量为y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 8.8g
$\frac{106}{x}=\frac{117}{y}=\frac{44}{8.8g}$
x=21.2g y=23.4g
样品中氯化钠的质量为:23g-21.2g=1.8g
故反应后氯化钠溶液的溶质质量分数为:$\frac{1.8g+23.4g}{23g+150g+135.8g-8.8g}$×100%=8.4%
答案:
(1)8.8;
(2)21.2
(3)所得到的溶液中溶质的质量分数为8.4%.
点评 本题主要考查化学方程式的书写和有关化学方程式的计算,完成此题,可以依据已有的知识进行.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
19.下列实验现象描述正确的是( )
| A. | 检验电解水实验负极产生的气体;产生蓝紫色火焰,放热 | |
| B. | 氧化铁与足量稀硫酸反应;红棕色固体逐渐减少至消失,溶液由无色变成黄色 | |
| C. | 加热氢氧化钠溶液与硫酸铜溶液反应后的物质,蓝色固体变成黑色的氧化铜 | |
| D. | 向氢氧化镁中加入无色酚酞溶液,无色酚酞溶液变成红色 |
15.新交规严禁酒驾,重铬酸钾(K2Cr207)可用于判定司机喝酒的多少.重铬酸钾(K2Cr207)中铬元素的化合价为( )
| A. | +7 | B. | +6 | C. | +4 | D. | +2 |
16.下列变化中,属于物理变化的是( )
| A. | 车胎爆炸 | B. | 食物变质 | ||
| C. | 葡萄糖在人体内氧化 | D. | 用富含淀粉的甘薯酿酒 |

 分析如图中A、B、C三种物质的溶解度曲线,回答问题.
分析如图中A、B、C三种物质的溶解度曲线,回答问题.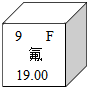 元素周期表中氟元素的有关信息如图所示,则氟的相对原子质量是19.00,氟原子的结构示意图为
元素周期表中氟元素的有关信息如图所示,则氟的相对原子质量是19.00,氟原子的结构示意图为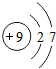 ,氟原子在化学反应中易得到(选填“得到”或”失去“)电子,由钠元素和氟元素组成的化合物氟化钠的化学式为NaF.
,氟原子在化学反应中易得到(选填“得到”或”失去“)电子,由钠元素和氟元素组成的化合物氟化钠的化学式为NaF.