题目内容
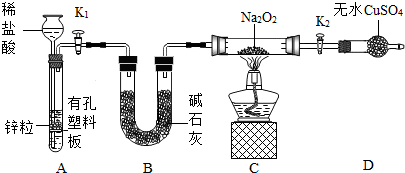
已知CuSO4是白色粉末,遇少量水可转化为蓝色晶体,在实验中常用于检验是否有少量的水存在,又知某气体X是由H2、CH4、CO中的一种或几种组成的,为了验证该气体的成分,现设计了如图所示的装置进行实验:

(1)若甲装置中CuO由黑色变成亮红色,乙装置中CuSO4不变色.丙装置中石灰水变浑浊,则气体X中一定有________,一定没有________,可能有________.
(2)若甲装置中CuO由黑色变成亮红色,乙装置中CuSO4变成蓝色,丙装置中石灰水无变化,则气体X中一定有________,一定没有________,可能有________.
(3)若甲装置中CuO由黑色变成亮红色,乙装置中CuSO4变成蓝色,丙装置中石灰水变浑浊,则气体X中一定有________,可能有________.
(4)试写出实验中可能发生反应的化学方程式________.
答案:
解析:
解析:
|
分析:首先三种气体H2、CH4和CO中有还原性的气体为H2和CO,与CuO可发生反应,从而使CuO还原成Cu.H2若与CuO反应后生成H2O,通过CuSO4的颜色改变来判断是否有水生成,从而可以确定气体X的成分中是否含有H2.CO与CuO反应后生成CO2,通过石灰水是否变浑浊来判断是否有CO2生成,进而可以推测气体X中是否含有CO,对于甲烷,由于它不与CuO反应,所以它就成为可能存在的气体. |

练习册系列答案
相关题目