题目内容
为了测定某赤铁矿石中氧化铁的质量分数,取矿石样品40g,加入盐酸,恰好完全反应时,共用去盐酸219g,过滤、洗涤、干燥后得滤渣8g(矿石中的杂质既不溶于水也不与盐酸反应).计算:(1)赤铁矿石中氧化铁的质量分数;
(2)盐酸的溶质质量分数;
(3)所得溶液的溶质质量分数.
【答案】分析:根据题意,赤铁矿石中的杂质既不溶于水也不与盐酸反应,则矿石反应后固体减少的质量为矿石中氧化铁的质量,进而计算出赤铁矿石中氧化铁的质量分数即可.
根据氧化铁与盐酸反应的化学方程式,由反应消耗氧化铁的质量计算出参加反应的HCl的质量、生成的氯化铁的质量,进而计算出盐酸的溶质质量分数、所得溶液的溶质质量分数即可.
解答:解:(1)赤铁矿石中氧化铁的质量为40g-8g=32g,
赤铁矿石中氧化铁的质量分数为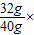 100%=80%.
100%=80%.
设盐酸中溶质的质量为x,生成氯化铁的质量为y,
6HCl+Fe2O3=2FeCl3+3H2O
219 160 325
x 32g y
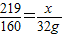 x=43.8g
x=43.8g
 y=65g
y=65g
(2)盐酸的溶质质量分数为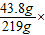 100%=20%.
100%=20%.
(3)所得溶液的溶质质量分数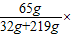 100%=25.9%.
100%=25.9%.
答:(1)赤铁矿石中氧化铁的质量分数为80%;
(2)盐酸的溶质质量分数为20%;
(3)所得溶液的溶质质量分数为25.9%.
点评:本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.
根据氧化铁与盐酸反应的化学方程式,由反应消耗氧化铁的质量计算出参加反应的HCl的质量、生成的氯化铁的质量,进而计算出盐酸的溶质质量分数、所得溶液的溶质质量分数即可.
解答:解:(1)赤铁矿石中氧化铁的质量为40g-8g=32g,
赤铁矿石中氧化铁的质量分数为
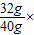 100%=80%.
100%=80%.设盐酸中溶质的质量为x,生成氯化铁的质量为y,
6HCl+Fe2O3=2FeCl3+3H2O
219 160 325
x 32g y
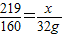 x=43.8g
x=43.8g y=65g
y=65g(2)盐酸的溶质质量分数为
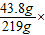 100%=20%.
100%=20%.(3)所得溶液的溶质质量分数
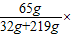 100%=25.9%.
100%=25.9%.答:(1)赤铁矿石中氧化铁的质量分数为80%;
(2)盐酸的溶质质量分数为20%;
(3)所得溶液的溶质质量分数为25.9%.
点评:本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
实验中学化学兴趣小组为了测定某赤铁矿石中Fe203的质量分数,取20克样品放入烧杯中,再取稀盐酸分五次加入烧杯中,每次均充分反应(杂质不溶于水,也不参加反应),测得实验数据如下:
| 次 数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入稀盐酸的质量(g) | 2l | 21 | 2l | 2l | 21 |
| 剩余固体的质量(g) | 16 | 12 | 8 | 4 | 4 |
(2)恰好完全反应时所得溶液中溶质的质量分数.
实验中学化学兴趣小组为了测定某赤铁矿石中Fe203的质量分数,取20克样品放 入烧杯中,再取稀盐酸分五次加入烧杯中,每次均充分反应(杂质不溶于水,也不参加反 应),测得实验数据如下:
| 次 数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入稀盐酸的质量(g) | 2l | 21 | 2l | 2l | 21 |
| 剩余固体的质量(g) | 16 | 12 | 8 | 4 | 4 |
求:(1)此赤铁矿石中Fe203的质量分数。
(2)恰好完全反应时所得溶液中溶质的质量分数。