题目内容
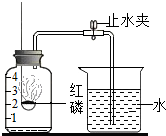 已知空气的主要成分是氮气和氧气.某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示:
已知空气的主要成分是氮气和氧气.某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示:(1)红磷在集气瓶中发生反应的化学方程式为:
(1)待燃烧停止,白烟消失并冷却后,打开止水夹,观察到烧杯中的水进入集气瓶,瓶内水面最终接近刻度l处.由此可知氧气约占空气总体积的
(3)若将红磷换成碳粉,该实验能否获得成功?
考点:空气组成的测定,书写化学方程式、文字表达式、电离方程式
专题:空气与水
分析:本题是测定空气中氧气的含量,我们常用燃烧红磷或白磷的方法,因为磷燃烧生成白色固体五氧化二磷,几乎不占空间,使得内外产生气压差,从而得到正确的结论.因此在选择可燃物时,必须考虑到:燃烧的条件;生成物的状态;不与空气中其他物质发生反应.保证本实验成功的关键是:①装置气密性好;②红磷要足量;③要冷却至室温再读数.
解答:解:
(1)红磷在氧气中燃烧生成五氧化二磷,反应的化学方程式为:4P+5O2
2P2O5.该实验中红磷稍过量,目的是将全部消耗掉集气瓶中内的氧气;
(2)根据烧杯中的水进入集气瓶,瓶内水面最终接近刻度1处可知,氧气约占空气体积的
;水倒流入集气瓶中的体积只有的
,若氮气易溶于水,则倒流入瓶内的水几乎会充满整个集气瓶,因此氮气是难溶于水的;红磷燃烧一会熄灭了,说明氮气不燃烧不支持燃烧,其化学性质不活泼;
(3)炭粉燃烧消耗氧气,同时生成二氧化碳气体,集气瓶内压强基本不变.故不能将红磷换成炭粉.
答案:
(1)4P+5O2
2P2O5 全部消耗掉集气瓶中内的氧气;
(2)
难溶于水
(3)否 碳粉燃烧生成CO2气体,瓶内气体体积无明显变化.
(1)红磷在氧气中燃烧生成五氧化二磷,反应的化学方程式为:4P+5O2
| ||
(2)根据烧杯中的水进入集气瓶,瓶内水面最终接近刻度1处可知,氧气约占空气体积的
| 1 |
| 5 |
| 1 |
| 5 |
(3)炭粉燃烧消耗氧气,同时生成二氧化碳气体,集气瓶内压强基本不变.故不能将红磷换成炭粉.
答案:
(1)4P+5O2
| ||
(2)
| 1 |
| 5 |
(3)否 碳粉燃烧生成CO2气体,瓶内气体体积无明显变化.
点评:本题主要考查用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,难度稍大.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
实验室内用常见方法制取下列各组气体时,气体发生装生相同的是( )
| A、氢气和氧气 |
| B、氢气和二氧化碳 |
| C、氧气和二氧化碳 |
| D、氢气、氧气和二氧化碳 |
下列物质不属于合金的是( )
| A、生铁 | B、白口铁 |
| C、氯化铁 | D、球墨铸铁 |
下列化学式或元素符号书写正确的是( )
| A、硫酸铁Fe2(SO4)3 |
| B、氧化钠NaO |
| C、氯化铜CuCl |
| D、铝AL |
能用来制氢气的装置是( )
| A、① | B、② | C、③ | D、④ |
 氮肥能促使作物的茎、叶生长茂盛,叶色浓绿.某同学发现她家 花盆中的花草生长迟缓,便施用了一种氮肥.如图是该氮肥包装标签的部分文字.试根据相关信息计算:
氮肥能促使作物的茎、叶生长茂盛,叶色浓绿.某同学发现她家 花盆中的花草生长迟缓,便施用了一种氮肥.如图是该氮肥包装标签的部分文字.试根据相关信息计算: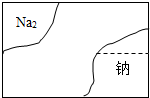 某探究学习小组在帮助实验员整理化学试剂时,发现一个盛有无色溶液的试剂瓶,标签破损(如图所示).已知它们是氯化钠、氢氧化钠、碳酸钠和硫酸钠四种溶液中的一种.请你对该试剂作出猜想,并设计实验验证.
某探究学习小组在帮助实验员整理化学试剂时,发现一个盛有无色溶液的试剂瓶,标签破损(如图所示).已知它们是氯化钠、氢氧化钠、碳酸钠和硫酸钠四种溶液中的一种.请你对该试剂作出猜想,并设计实验验证.