题目内容
16.将12g镁与铁的混合物投入足量稀盐酸中充分反应,生成气体的质量可能是( )| A. | 0.4g | B. | 0.8g | C. | 1.0g | D. | 1.2g |
分析 铁和稀盐酸反应生成氯化亚铁和氢气,镁和稀盐酸反应生成氯化镁和氢气,根据铁和镁的质量和可以计算生成氢气的质量范围.
解答 解:设12g铁和稀盐酸生成氢气的质量为x,12g镁和稀盐酸反应生成氢气的质量为y,
Fe+2HCl═FeCl2+H2↑,Mg+2HCl═MgCl2+H2↑,
56 2 24 2
12g x 12g y
$\frac{56}{12g}$=$\frac{2}{x}$,$\frac{24}{12g}$=$\frac{2}{y}$,
x=0.43g,y=1g,
由计算可知,当12克铁和镁的混合物与足量盐酸反应,反应后生成氢气的质量大于0.43g,小于1g;
故选:B.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
6.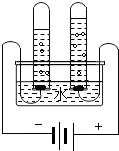 如图为验证水的组成的实验装置,下列有关说法正确的是( )
如图为验证水的组成的实验装置,下列有关说法正确的是( )
 如图为验证水的组成的实验装置,下列有关说法正确的是( )
如图为验证水的组成的实验装置,下列有关说法正确的是( )| A. | 正极和负极产生的气体质量比为1:2 | |
| B. | 正极产生的气体能使带火星的木条复燃 | |
| C. | 水是由一个氧元素和两个氢元素组成的 | |
| D. | 该变化中的最小粒子为氢分子和氧分子 |
7.下列有关碳和碳的氧化物的说法错误的是( )
| A. | 金刚石和石墨的物理性质不同,是因为它们的碳原子排列方式不同 | |
| B. | 一氧化碳和二氧化碳的组成元素相同,所以它们的化学性质相似 | |
| C. | 木炭和活性炭都具有吸附性 | |
| D. | 二氧化碳用于灭火,即利用它的物理性质也利用了它的化学性质 |
11.不锈钢是铁的合金,与纯铁相比,不锈钢最重要的特性是( )
| A. | 密度小 | B. | 光泽好 | C. | 导电性强 | D. | 抗腐蚀性强 |
8.今年春季,我省部分地区雨水较少,出现了旱情,为了增强农作物的抗旱能力,小明建议父母施用适量的磷肥,下列化肥中属于磷肥的是( )
| A. | K2SO4 | B. | CO(NH2)2 | C. | Ca3(PO4)2 | D. | KNO3 |
6.下列有关实验的叙述错误的是( )
| A. | 用pH试纸测定未知溶液的酸碱度时,应将pH试纸预先用水湿润 | |
| B. | 实验室用高锰酸钾制取O2,在实验结束时应先将导管移出水面,再停止加热 | |
| C. | 稀释浓硫酸时,要把浓硫酸缓缓注入盛有水的烧杯中,用玻璃棒引流并不断搅拌 | |
| D. | 在粗盐提纯实验中,待蒸发皿中出现较多固体时,停止加热,利用余热将滤液蒸干 |

 甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题:
甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题: