题目内容
某实验小组利用废硫酸液制备K2SO4 晶体,其制取流程如下:
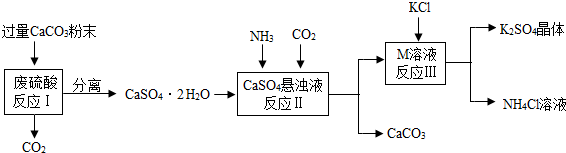
请根据上述流程,回答下列问题:
(1)反应Ⅲ中相关物质的溶解度如表所示.你认为反应Ⅲ在常温下能实现的原因是 .
(2)用饱和K2SO4溶液而不用水来洗涤反应Ⅲ所得晶体的目的是 ;
(3)关于该反应,下列说法正确的是
A.反应Ⅰ中,将CaCO3 研成粉末的目的是增大接触面积,是反应充分
B.整个过程中,只有一种物质可循环利用
C.本流程涉及反应都可以在常温下进行,能耗小
D.为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入过量的Ba(NO3)2 溶液,振荡、静置,再向上层清液中滴加AgNO3溶液,观察现象即可判断.

请根据上述流程,回答下列问题:
(1)反应Ⅲ中相关物质的溶解度如表所示.你认为反应Ⅲ在常温下能实现的原因是
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(3)关于该反应,下列说法正确的是
A.反应Ⅰ中,将CaCO3 研成粉末的目的是增大接触面积,是反应充分
B.整个过程中,只有一种物质可循环利用
C.本流程涉及反应都可以在常温下进行,能耗小
D.为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入过量的Ba(NO3)2 溶液,振荡、静置,再向上层清液中滴加AgNO3溶液,观察现象即可判断.
考点:物质的相互转化和制备,盐的化学性质
专题:物质的制备
分析:解答此类题目时要反复阅读题意,明确题目的要求和前后的关联,然后进行解答.
(1)从生成物的溶解度大小考虑反应能否发生;
(2)结合实验目的分析洗涤的方法;
(3)把反应物研成粉末是为了加快反应速率,如果生成物和反应物中都有某种物质,这种物质一般可循环利用;检验氯离子时要排除硫酸根的干扰逐项分析判断.
(1)从生成物的溶解度大小考虑反应能否发生;
(2)结合实验目的分析洗涤的方法;
(3)把反应物研成粉末是为了加快反应速率,如果生成物和反应物中都有某种物质,这种物质一般可循环利用;检验氯离子时要排除硫酸根的干扰逐项分析判断.
解答:解:(1)根据复分解反应发生的条件,反应Ⅲ中随没有不溶物,但常温下K2SO4的溶解度小,在生成物中会以沉淀的形式出现,故反应可以进行.故填:常温下K2SO4的溶解度小;
(2)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是减少K2SO4的溶解;故填:减少K2SO4的溶解;
(3)A、将CaCO3研成粉末,可以增大反应物的接触面积,其目的是加快反应速率.故正确;
B、观察上述流程,发现二氧化碳和碳酸钙既是反应物也是生成物,故可循环使用的物质有CO2和CaCO3.故错误;
C、本流程涉及反应都可以在常温下进行,能耗小,故正确;
D、为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入过量的Ba(NO3)2溶液,振荡、静置,目的是除去硫酸根,再向上层清液中滴加AgNO3溶液,如果没有白色沉淀,说明洗涤干净.故正确;
故正确的选项为:ABD.
(2)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是减少K2SO4的溶解;故填:减少K2SO4的溶解;
(3)A、将CaCO3研成粉末,可以增大反应物的接触面积,其目的是加快反应速率.故正确;
B、观察上述流程,发现二氧化碳和碳酸钙既是反应物也是生成物,故可循环使用的物质有CO2和CaCO3.故错误;
C、本流程涉及反应都可以在常温下进行,能耗小,故正确;
D、为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入过量的Ba(NO3)2溶液,振荡、静置,目的是除去硫酸根,再向上层清液中滴加AgNO3溶液,如果没有白色沉淀,说明洗涤干净.故正确;
故正确的选项为:ABD.
点评:此题全面考查了学生对知识的掌握和应用能力,难度比较大,解答时一定要注意知识的前后的联系和综合运用.

练习册系列答案
相关题目
下列实验操作正确的是( )
A、 加热液体 |
B、 读取液体 |
C、 倾倒液体 |
D、 检查装置气密性 |
质量相同的下列物质,在氧气中完全燃烧,消耗氧气最多的是( )
| A、H2 | B、Fe |
| C、S | D、C |
在A+B═C+D反应中,若25gA与10gB恰好完全反应生成5gC,则10gA与足量B反应,可生成D的质量是( )
| A、4g | B、8g |
| C、10g | D、12g |

