题目内容
5. 向CuSO4溶液中先后逐滴滴加100g Ba(OH)2溶液与一定量的HCl溶液,反应过程中加入溶液的质量与产生沉淀质量关系如图所示.下列说法正确的是( )
向CuSO4溶液中先后逐滴滴加100g Ba(OH)2溶液与一定量的HCl溶液,反应过程中加入溶液的质量与产生沉淀质量关系如图所示.下列说法正确的是( )| A. | o~a溶液导电性逐渐增强 | |
| B. | d点溶质的成分为一种 | |
| C. | m=3.31 | |
| D. | 原Ba(OH)2溶液的溶质质量分数为1.71% |
分析 根据硫酸铜和氢氧化钡反应生成硫酸钡沉淀和氢氧化铜沉淀,硫酸钡沉淀不溶于酸,氢氧化铜和盐酸反应生成氯化铜和水,依据图象中的数据进行分析.
解答 解:A、通过分析图象可知,o~a是氢氧化钡和硫酸铜反应生成硫酸钡沉淀和氢氧化铜沉淀,溶液导电性逐渐减弱,故A错误;
B、d点表示加入的盐酸是过量的,盐酸和氢氧化铜反应生成氯化铜和水,所以溶质的成分为:氯化铜和氯化氢两种,故B错误;
C、由图象中的数据可知生成硫酸钡沉淀的质量为2.33g,
设生成氢氧化铜沉淀的质量为x,参加反应的氢氧化钡的质量为y
CuSO4+Ba(OH)2=Cu(OH)2↓+BaSO4↓
171 94 233
y x 2.33g
$\frac{171}{y}$=$\frac{94}{x}$=$\frac{233}{2.33g}$
x=0.94g
y=1.71g
所以m=0.94g+2.33g=3.27g,故C错误;
D、Ba(OH)2溶液的溶质质量分数为:$\frac{1.71g}{100g}$×100%=1.71%,故D正确.
故选:D.
点评 本题属于实验探究题,综合性较强,既有实验探究,又有实验数据图象的分析,只有综合掌握了基础知识才能较好的完成本类练习题.

练习册系列答案
相关题目
12.生活中处处有化学,下列生活、生产中的变化,属于化学变化的是( )
| A. |  海水晒盐 | B. |  葡萄酿酒 | C. |  雕琢玉石 | D. |  灯泡发光 |
16.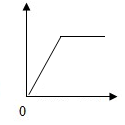 下列各选项与如图所示曲线相符的是( )
下列各选项与如图所示曲线相符的是( )
 下列各选项与如图所示曲线相符的是( )
下列各选项与如图所示曲线相符的是( )| 选项 | 横坐标 | 纵坐标 |
| A | 加热高锰酸钾制取氧气 | 氧元素的质量分数 |
| B | 向一定量的氢氧化钠和碳酸钠混合溶液中加入稀盐酸的质量 | 产 生气体的质量 |
| C | 向一定量的澄清石灰水中加入碳酸钠溶液的质量 | 生成沉淀的质量 |
| D | 向一定量的铁粉中加入硫酸铜溶液 | 溶液的质量 |
| A. | A | B. | B | C. | C | D. | D |
13.下列属于物理变化的是( )
| A. | 食物腐败 | B. | 钢铁生锈 | C. | 干冰升华 | D. | 酒精燃烧 |
10.化学用语是学习和交流化学知识的通用语言,以下符号所表示的意义最多的是( )
| A. | O | B. | CO32- | C. | S | D. | 3SO2 |
17.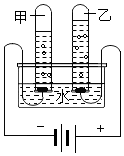 有关电解水的实验如图所示,下列叙述错误的是( )
有关电解水的实验如图所示,下列叙述错误的是( )
 有关电解水的实验如图所示,下列叙述错误的是( )
有关电解水的实验如图所示,下列叙述错误的是( )| A. | 水由氢气和氧气组成 | B. | 水由氢元素和氧元素组成 | ||
| C. | 试管甲中的气体是氢气 | D. | 试管乙中的气体是氧气 |
14.下列化学反应及反应类型与如图所示的微观变化对应的是( )


| A. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2化合反应 | |
| B. | 2HI+Cl2═2HCl+I2 置换反应 | |
| C. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ 分解反应 | |
| D. | 2HCl+CuO═CuCl2+H2O 复分解反应 |
15.科学家最近发现,通过简单的化学反应,可以将树木纤维素转变成超级储能装置,如图是该反应的围观示意图,下列说法错误的是( )
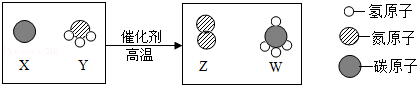

| A. | X、Y、Z、W四种物质中有三种物质是由分子构成的 | |
| B. | W物质中碳元素的质量分数为75% | |
| C. | 参加反应的X、Y两物质的粒子个数比为1:1 | |
| D. | 该反应属于置换反应 |
