题目内容
 某有机物在氧气中充分燃烧,将生成的水蒸气、二氧化碳气体依次通过装置甲和乙 (假设每步吸收完全),称量通入气体前后装置的质量,数据如下:
某有机物在氧气中充分燃烧,将生成的水蒸气、二氧化碳气体依次通过装置甲和乙 (假设每步吸收完全),称量通入气体前后装置的质量,数据如下:
| 装置甲 | 装置乙 | |
| 通气前质量 | 200g | 180g |
| 通气后质量 | 203.6g | 184,4g |
- A.CH4
- B.C2H4
- C.C2H5OH
- D.CH3OH
AD
分析:依据浓硫酸能吸收水蒸气,而氢氧化钠能吸收二氧化碳,所以装置甲的增重为反应生成水的质量,装置乙的增重为反应生成的二氧化碳的质量,依据质量守恒定律可知该有机物中的碳元素与生成的二氧化碳中的碳元素质量相等,该有机物中的氢元素与生成的水中的氢元素质量相等,因此可计算出有机物中碳和氢元素的质量比,进而可得碳原子与氢原子的个数比,从而可判断可能的化学式;
解答:由于浓硫酸能吸收水蒸气,而氢氧化钠能吸收二氧化碳,所以装置甲的增重为反应生成水的质量,其质量为203.6g-200g=3.6g;装置乙的增重为反应生成的二氧化碳的质量,其质量为184.4g-180g=4.4g;依据质量守恒定律可知该有机物中的碳元素与生成的二氧化碳中的碳元素质量相等,该有机物中的氢元素与生成的水中的氢元素质量相等,因此可得该有机物中氢和碳元素的质量比为 =
= ,所以该有机物中氢碳原子的个数比是
,所以该有机物中氢碳原子的个数比是 =
= ,分析选项中各有机物的化学式可知CH4、CH3OH符合该有机物中碳氢的原子个数比;
,分析选项中各有机物的化学式可知CH4、CH3OH符合该有机物中碳氢的原子个数比;
故选AD
点评:解答本题的关键是浓硫酸质量的增加量就是生成水的质量,氢氧化钠溶液质量的增加量就是生成的二氧化碳的质量.
分析:依据浓硫酸能吸收水蒸气,而氢氧化钠能吸收二氧化碳,所以装置甲的增重为反应生成水的质量,装置乙的增重为反应生成的二氧化碳的质量,依据质量守恒定律可知该有机物中的碳元素与生成的二氧化碳中的碳元素质量相等,该有机物中的氢元素与生成的水中的氢元素质量相等,因此可计算出有机物中碳和氢元素的质量比,进而可得碳原子与氢原子的个数比,从而可判断可能的化学式;
解答:由于浓硫酸能吸收水蒸气,而氢氧化钠能吸收二氧化碳,所以装置甲的增重为反应生成水的质量,其质量为203.6g-200g=3.6g;装置乙的增重为反应生成的二氧化碳的质量,其质量为184.4g-180g=4.4g;依据质量守恒定律可知该有机物中的碳元素与生成的二氧化碳中的碳元素质量相等,该有机物中的氢元素与生成的水中的氢元素质量相等,因此可得该有机物中氢和碳元素的质量比为
 =
= ,所以该有机物中氢碳原子的个数比是
,所以该有机物中氢碳原子的个数比是 =
= ,分析选项中各有机物的化学式可知CH4、CH3OH符合该有机物中碳氢的原子个数比;
,分析选项中各有机物的化学式可知CH4、CH3OH符合该有机物中碳氢的原子个数比;故选AD
点评:解答本题的关键是浓硫酸质量的增加量就是生成水的质量,氢氧化钠溶液质量的增加量就是生成的二氧化碳的质量.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某有机物在氧气中充分燃烧后,产生只有二氧化碳和水,甲、乙两组同学分别用下图两种方法测定它的组成.请你分析,并参与测定工作;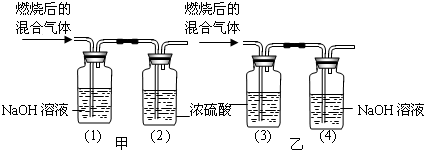
(1)你选用的实验装置是 (“甲”或“乙”),你不选另一个装置的原因是 .
(2)根据表中数据,推测出该有机物是由 元素组成的,各元素的质量比为 (假设实验过程中气体均全部被吸收).
提示:浓硫酸可以吸收水蒸气,氢氧化钠可以吸收二氧化碳.

| 燃烧有机物的质量 | 实验装置 | 实验(1)~(4)装置质量 | ||
| 实验前 | 实验后 | |||
| 甲组 | 1.6g | 甲 | (1)150g | (1)154.6g |
| (2)150g | (1)153.4g | |||
| 乙组 | 1.6g | 乙 | (3)150g | (1)153.6g |
| (4)150g | (1)154.4g | |||
(2)根据表中数据,推测出该有机物是由
提示:浓硫酸可以吸收水蒸气,氢氧化钠可以吸收二氧化碳.
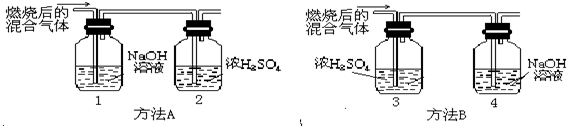
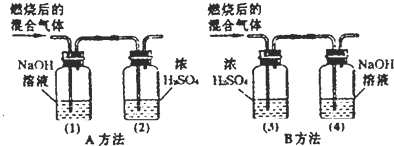 (2005?青浦区)某有机物在氧气中充分燃烧后,产物只有二氧化碳和水.甲、乙两组同学分别用A、两种方法(为如图所示)测定它的组成,得到两组数据(见下表).请你分析:浓H2SO4具有
(2005?青浦区)某有机物在氧气中充分燃烧后,产物只有二氧化碳和水.甲、乙两组同学分别用A、两种方法(为如图所示)测定它的组成,得到两组数据(见下表).请你分析:浓H2SO4具有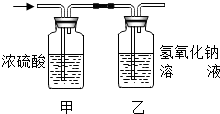 (2012?牡丹江)某有机物在氧气中充分燃烧,将生成的水蒸气、二氧化碳气体依次通过装置甲和乙 (假设每步吸收完全),称量通入气体前后装置的质量,数据如下:
(2012?牡丹江)某有机物在氧气中充分燃烧,将生成的水蒸气、二氧化碳气体依次通过装置甲和乙 (假设每步吸收完全),称量通入气体前后装置的质量,数据如下: