题目内容
13. 如图是用红磷在空气中燃烧来测定空气中氧气含量实验.具体过程如下:
如图是用红磷在空气中燃烧来测定空气中氧气含量实验.具体过程如下:第一步:在集气瓶中加入少量水,并将水面上方的容积划分为五等份,做好标记.
第二步:点燃燃烧匙内的红磷,伸入集气瓶中,把塞子塞紧.
第三步:待红磷熄灭并冷却后,打开弹簧夹,观察现象.
请回答下列问题:
(1)上面实验中红磷燃烧的现象是:红磷燃烧产生大量白烟,放出热量;
(2)发生反应的文字表达式是:磷+氧气$\stackrel{点燃}{→}$五氧化二磷;
(3)该实验得出的正确结论是:空气中氧气约占总体积的$\frac{1}{5}$;
(4)如果操作不当,测得的实验值比实际的偏小,请你分析其中可能的原因:红磷的量不够;装置可能漏气;未冷却到室温就打开弹簧夹(任意写出一条即可);
(5)实验开始前先在集气瓶中加入少量水的目的是:降温和吸收五氧化二磷,防止污染空气.
分析 (1)根据红磷燃烧的现象分析解答;
(2)根据磷与氧气在点燃条件下反应生成五氧化二磷解答;
(3)红磷与氧气反应生成固体,消耗了瓶内的气体,压强减小,外界大气压会压着水进入集气瓶;
(4)保证本实验成功的关键是:①装置气密性好;②红磷要足量;③要冷却至室温再读数.
(5)根据实验开始前先在集气瓶中加入少量水的目的是:降温和吸收五氧化二磷,防止污染空气解答.
解答 解:(1)实验中观察到的现象是:红磷燃烧产生大量白烟,放出热量.
(2)磷与氧气在点燃条件下反应生成五氧化二磷.该反应的文字表达式为:磷+氧气$\stackrel{点燃}{→}$五氧化二磷;
(3)打开弹簧夹后,有水进入集气瓶,水位上升约 $\frac{1}{5}$,说明氧气约占空气总体积的$\frac{1}{5}$;
(4)进行此实验时,必须保证装置的气密性良好,红磷足量,瓶子冷却后再打开弹簧夹,否则会导致结果不准确,所以本题答案为:红磷的量不够;装置可能漏气;未冷却到室温就打开弹簧夹.
(5)实验开始前先在集气瓶中加入少量水的目的是:降温和吸收五氧化二磷,防止污染空气.
故答案为:
(1)产生大量的白烟,放出热量;
(2)磷+氧气$\stackrel{点燃}{→}$五氧化二磷;
(3)$\frac{1}{5}$;
(4)红磷的量不够;装置可能漏气;未冷却到室温就打开弹簧夹.
(5)降温和吸收五氧化二磷,防止污染空气
点评 本题主要考查测定空气里氧气含量的探究实验,该实验的结论和实验中注意事项是考查重点,要知道造成实验结果不准确的原因:红磷量不足,或装置漏气,或没有冷却至室温就测量就会造成测量值偏小.

练习册系列答案
相关题目
4.下列方法中,相比较得到的水最纯的是( )
| A. | 吸附 | B. | 沉淀 | C. | 过滤 | D. | 蒸馏 |
1.下列实验操作错误的是( )
| A. | 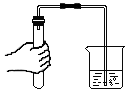 | B. | 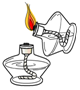 | C. | 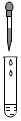 | D. |  |
3.维生素C(C6H8O6)主要存在于蔬菜和水果中,它能促进人体生长发育,增强人体对疾病的抵抗力.近年来科学家发现维生素C有防癌的作用.关于维生素C,下列说法正确的是( )
| A. | 维生素C中C、H、O三种元素的质量比为3:4:3 | |
| B. | 维生素C是氧化物 | |
| C. | 一个维生素C分子由6个碳原子、8个氢原子和6个氧原子构成 | |
| D. | 维生素C是由6个碳元素、8个氢元素和6个氧元素组成 |
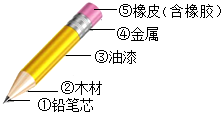 如图是同学们经常使用的铅笔示意图.
如图是同学们经常使用的铅笔示意图.
 如图是电解水的装置,回答问题.
如图是电解水的装置,回答问题.