题目内容
元素周期表是学习化学的重要工具,下表是元素周期表的一部分.| 族 周期 | ⅠA | |||||||
| 1 | 1 H 氢 1.008 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | ||||
| 3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 铝 |
(1)13号元素符号是 ,11号元素在化学变化中 (填“易得电子”或“易失电子”).
(2)9号元素的原子结构示意图为,其中X为 ,
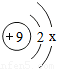 请画出该元素形成的离子结构示意图
请画出该元素形成的离子结构示意图 (3)由1号元素和8号元素组成的阴离子符号为 ,由11、6和8号元素组成物质的化学式为 .
【答案】分析:(1)根据元素周期表结合原子最外层电子数的特点进行解答;
(2)根据在原子中,原子序数=质子数=核电荷数=核外电子数,进行解答;
根据非金属元素易得到电子,形成阴离子;达到8个电子的稳定结构;进行解答;
(3)根据1号元素和8号元素分别是H,O,组成的阴离子符号即可解答;
根据1、6、7和8号元素分别是H,C,N,O,组成的盐的化学式即可解答.
解答:解:(1)由元素周期表可知13号元素是铝,其符号是Al;11号元素是钠,钠原子的最外层电子数是1,在化学变化中容易失去电子;
故答案为:Al;易失电子;
(2)9号元素是氟元素,根据在原子中,原子序数=质子数=核电荷数=核外电子数,可得9=2+x,x=7;
根据非金属元素易得到电子,形成阴离子,从而达到8个电子的稳定结构,所以该离子的结构示意图为: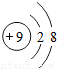
故答案为:7;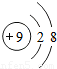 ;
;
(3)根据1号元素和8号元素分别是H,O,组成的阴离子符号为:OH-;
根据11、6和8号元素分别是Na,C,O,组成的物质的化学式为:Na2CO3;
故答案为:OH-; Na2CO3.
点评:本题考查学生根据元素周期表知识进行综合分析解题的能力.
(2)根据在原子中,原子序数=质子数=核电荷数=核外电子数,进行解答;
根据非金属元素易得到电子,形成阴离子;达到8个电子的稳定结构;进行解答;
(3)根据1号元素和8号元素分别是H,O,组成的阴离子符号即可解答;
根据1、6、7和8号元素分别是H,C,N,O,组成的盐的化学式即可解答.
解答:解:(1)由元素周期表可知13号元素是铝,其符号是Al;11号元素是钠,钠原子的最外层电子数是1,在化学变化中容易失去电子;
故答案为:Al;易失电子;
(2)9号元素是氟元素,根据在原子中,原子序数=质子数=核电荷数=核外电子数,可得9=2+x,x=7;
根据非金属元素易得到电子,形成阴离子,从而达到8个电子的稳定结构,所以该离子的结构示意图为:
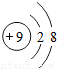
故答案为:7;
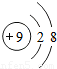 ;
;(3)根据1号元素和8号元素分别是H,O,组成的阴离子符号为:OH-;
根据11、6和8号元素分别是Na,C,O,组成的物质的化学式为:Na2CO3;
故答案为:OH-; Na2CO3.
点评:本题考查学生根据元素周期表知识进行综合分析解题的能力.

练习册系列答案
相关题目
 ,第3周期中某元素与氧元素的化学性质相似,该元素的原子结构示意图为
,第3周期中某元素与氧元素的化学性质相似,该元素的原子结构示意图为  ,则x=
,则x=
 元素周期表是学习化学的重要工具,图是元素周期表中的一格,从该图中,我们获取的相关信息中错误的是( )
元素周期表是学习化学的重要工具,图是元素周期表中的一格,从该图中,我们获取的相关信息中错误的是( ) 元素周期表是学习化学的重要工具.如图是元素周期表中的一格,从中获取的信息错误的是( )
元素周期表是学习化学的重要工具.如图是元素周期表中的一格,从中获取的信息错误的是( )