题目内容
棉花是一种天然纤维(仅含C、H元素),某兴趣小组对棉花样品中所含元素进行实验验证.他们在氧气中燃烧棉花,通过观察反应现象、对生成物进行检验得出结论.另外对装置内的反应剩余物进行回收.
实验所需的试剂和样品为氯酸钾(KClO3)、二氧化锰(MnO2)、澄清石灰水[主要成分Ca(OH)2]、少量干燥的棉花.
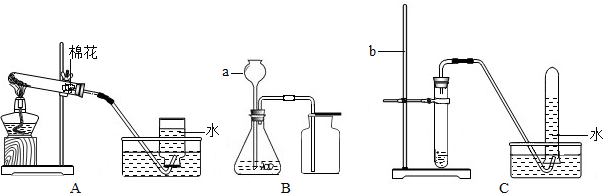
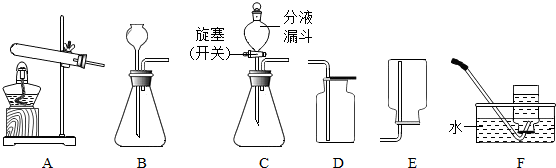
如图所列的是一些常见的实验装置和基本操作:
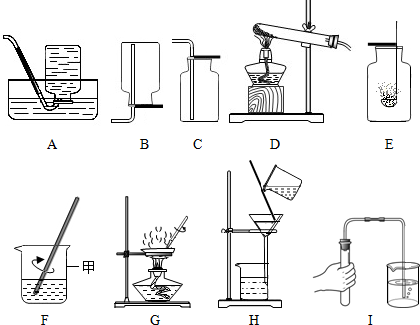
回答下列问题:
(1)仪器甲是 ,I操作叫做 .
(2)用D装置制取氧气,反应的化学方程式为 .
(3)在完全反应后,试管中的混合物是 .
分离并得到上述物质必要的操作是 (用字母按操作顺序填写).
(4)将在空气中点燃的棉花迅速伸入盛满氧气的冷而干燥的集气瓶中,待
燃烧完成后,证明棉花中含有氢元素的实验现象是 .检出含有碳元素所需的试剂是 .
(5)本实验中收集氧气你所选用的操作方法是 (填字母).某同学只用一瓶氧气检出棉花由碳、氢元素组成的结论.你认为该同学先检出碳元素还是氢元素?请说出你的理由: .
实验所需的试剂和样品为氯酸钾(KClO3)、二氧化锰(MnO2)、澄清石灰水[主要成分Ca(OH)2]、少量干燥的棉花.
如图所列的是一些常见的实验装置和基本操作:

回答下列问题:
(1)仪器甲是
(2)用D装置制取氧气,反应的化学方程式为
(3)在完全反应后,试管中的混合物是
分离并得到上述物质必要的操作是
(4)将在空气中点燃的棉花迅速伸入盛满氧气的冷而干燥的集气瓶中,待
燃烧完成后,证明棉花中含有氢元素的实验现象是
(5)本实验中收集氧气你所选用的操作方法是
考点:实验探究物质的组成成分以及含量,混合物的分离方法,常见气体的检验与除杂方法,实验室制取氧气的反应原理,质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)要熟悉各种仪器的名称、用途和使用方法;
凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
(2)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;
(3)二氧化锰在氯酸钾分解的反应中做催化剂;
分离氯化钾和二氧化锰时,需要通过溶解、过滤、蒸发的步骤进行;
(4)根据实验现象可以判断棉花的元素组成;
(5)氧气的密度比空气的密度大,不易溶于水;
如果先通过澄清石灰水检验碳元素,则会影响对氢元素的判断.
凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
(2)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;
(3)二氧化锰在氯酸钾分解的反应中做催化剂;
分离氯化钾和二氧化锰时,需要通过溶解、过滤、蒸发的步骤进行;
(4)根据实验现象可以判断棉花的元素组成;
(5)氧气的密度比空气的密度大,不易溶于水;
如果先通过澄清石灰水检验碳元素,则会影响对氢元素的判断.
解答:解:(1)仪器甲是烧杯,I操作叫做检查装置的气密性.
故填:烧杯;检查装置的气密性.
(2)用D装置制取氧气,反应的化学方程式为:2KClO3
2KCl+3O2↑.
故填:2KClO3
2KCl+3O2↑.
(3)在完全反应后,试管中的混合物是氯化钾和二氧化锰;
分离并得到上述物质必要的操作是溶解、过滤和蒸发,即通过FHG的操作顺序进行.
故填:氯化钾和二氧化锰;FHG.
(4)将在空气中点燃的棉花迅速伸入盛满氧气的冷而干燥的集气瓶中,待燃烧完成后,证明棉花中含有氢元素的实验现象是集气瓶内壁出现水雾;
检出含有碳元素所需的试剂是澄清石灰水,向棉花燃烧完成后的集气瓶中加入适量的澄清石灰水,澄清石灰水变浑浊,说明生成了二氧化碳,进一步说明棉花中含有碳元素.
故填:集气瓶内壁出现水雾;澄清石灰水.
(5)可以利用向上排空气法或排水法收集氧气,本实验中收集氧气应该是干燥的,因此所选用的收集方法是向上排空气法,即利用C装置收集;
应该先检验氢元素,因为如果先向集气瓶中加入澄清石灰水时,虽然能够证明棉花中含有碳元素,但是无法检验棉花中是否含有氢元素了.
故填:先检出氢元素,棉花燃烧完成后,集气瓶内壁出现水雾,说明生成了水,进一步说明棉花中含有氢元素;
再向集气瓶中加入适量的澄清石灰水,澄清石灰水变浑浊,说明生成了二氧化碳,进一步说明棉花中含有碳元素.
故填:烧杯;检查装置的气密性.
(2)用D装置制取氧气,反应的化学方程式为:2KClO3
| ||
| △ |
故填:2KClO3
| ||
| △ |
(3)在完全反应后,试管中的混合物是氯化钾和二氧化锰;
分离并得到上述物质必要的操作是溶解、过滤和蒸发,即通过FHG的操作顺序进行.
故填:氯化钾和二氧化锰;FHG.
(4)将在空气中点燃的棉花迅速伸入盛满氧气的冷而干燥的集气瓶中,待燃烧完成后,证明棉花中含有氢元素的实验现象是集气瓶内壁出现水雾;
检出含有碳元素所需的试剂是澄清石灰水,向棉花燃烧完成后的集气瓶中加入适量的澄清石灰水,澄清石灰水变浑浊,说明生成了二氧化碳,进一步说明棉花中含有碳元素.
故填:集气瓶内壁出现水雾;澄清石灰水.
(5)可以利用向上排空气法或排水法收集氧气,本实验中收集氧气应该是干燥的,因此所选用的收集方法是向上排空气法,即利用C装置收集;
应该先检验氢元素,因为如果先向集气瓶中加入澄清石灰水时,虽然能够证明棉花中含有碳元素,但是无法检验棉花中是否含有氢元素了.
故填:先检出氢元素,棉花燃烧完成后,集气瓶内壁出现水雾,说明生成了水,进一步说明棉花中含有氢元素;
再向集气瓶中加入适量的澄清石灰水,澄清石灰水变浑浊,说明生成了二氧化碳,进一步说明棉花中含有碳元素.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目



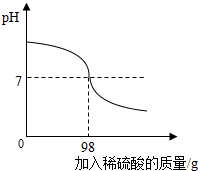 造纸厂生产会产生含氢氧化钠的废水,需经处理呈中性后排放.为测定此废水中氢氧化钠的质量分数,小华取80g废水样品加入到锥形瓶中,逐滴加入10%的稀硫酸,如图所示.
造纸厂生产会产生含氢氧化钠的废水,需经处理呈中性后排放.为测定此废水中氢氧化钠的质量分数,小华取80g废水样品加入到锥形瓶中,逐滴加入10%的稀硫酸,如图所示.