题目内容
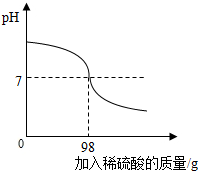 造纸厂生产会产生含氢氧化钠的废水,需经处理呈中性后排放.为测定此废水中氢氧化钠的质量分数,小华取80g废水样品加入到锥形瓶中,逐滴加入10%的稀硫酸,如图所示.
造纸厂生产会产生含氢氧化钠的废水,需经处理呈中性后排放.为测定此废水中氢氧化钠的质量分数,小华取80g废水样品加入到锥形瓶中,逐滴加入10%的稀硫酸,如图所示.(1)恰好完全反应时,所加稀硫酸的质量为
(2)计算废水中氢氧化钠的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:利用恰好完全反应所消耗硫酸的质量,根据反应的化学方程式,计算废水中氢氧化钠的质量,最后利用溶液中溶质的质量分数公式计算出废水中氢氧化钠的质量分数.
解答:解:(1)由图可知,恰好反应时,pH=7,所加稀硫酸的质量为98g;
故填:98;
(2)解:反应消耗硫酸的质量为:98g×10%=9.8g,
设废水样品中氢氧化钠的质量为x.
2NaOH+H2SO4=Na2SO4+2H2O
80 98
x 9.8g
=
x=8g
废水中氢氧化钠的质量分数为
×100%=10%
答:废水中氢氧化钠的质量分数为10%.
故填:98;
(2)解:反应消耗硫酸的质量为:98g×10%=9.8g,
设废水样品中氢氧化钠的质量为x.
2NaOH+H2SO4=Na2SO4+2H2O
80 98
x 9.8g
| 80 |
| 98 |
| x |
| 9.8g |
x=8g
废水中氢氧化钠的质量分数为
| 8g |
| 80g |
答:废水中氢氧化钠的质量分数为10%.
点评:根据质量守恒定律,反应后溶液的质量与所加入稀硫酸的质量差即所取废水溶液的质量.

练习册系列答案
相关题目
下列说法正确的是( )
| A、有机物一定含碳元素,所以金刚石、碳酸钙、乙醇都属于有机物 |
| B、水果富含纤维素,几乎不含脂肪和蛋白质,因而可以无节制地放心食用 |
| C、C、CO、H2都具有还原性,所以它们都可以与Fe2O3发生置换反应 |
| D、只要均衡膳食,不挑食、不偏食,人体就不会缺乏各种营养元素 |
