题目内容
13.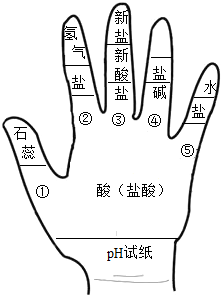 构建模型和构建知识网络是化学学习中重要的学习方法,某同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:
构建模型和构建知识网络是化学学习中重要的学习方法,某同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:①酸溶液具有相似的化学性质是因为都含有H+微粒(填符号).
②图中①的现象是紫色石蕊溶液变红色.
③如用湿润的pH试纸测定盐酸的pH,则结果会偏大(填“偏大”“偏小”、“无影响”).
④氢氧化铝可用于治疗胃酸过多,写出反应的化学方程式Al(OH)3+3HCl═AlCl3+3H2O.
分析 ①根据酸是指在电离时产生的阳离子全部是氢离子的化合物,进行分析解答.
②紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝.
③用湿润的pH试纸测定盐酸的pH,再蘸取待测液滴在pH试纸上,稀释了待测溶液,使溶液的酸性减弱,进行分析解答.
④根据氢氧化铝与盐酸反应生成氯化铝和水,写出反应的化学方程式即可.
解答 解:①酸是指在电离时产生的阳离子全部是氢离子的化合物,酸溶液具有相似的化学性质是因为都含有氢离子,其离子符号为:H+.
②紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝,盐酸显酸性,能使紫色石蕊溶液变红色.
③用湿润的pH试纸测定盐酸的pH,再蘸取待测液滴在pH试纸上,稀释了待测溶液,使溶液的酸性减弱,当溶液的pH小于7时,呈酸性,且pH越小,酸性越强,则测得的pH结果比实际值偏大.
④氢氧化铝与盐酸反应生成氯化铝和水,反应的化学方程式为:Al(OH)3+3HCl═AlCl3+3H2O.
故答案为:①H+;②紫色石蕊溶液变红色;③偏大;④Al(OH)3+3HCl═AlCl3+3H2O.
点评 本题难度不大,掌握酸的化学性质(能与酸碱指示剂、活泼金属、金属氧化物、碱、盐等反应)并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
4.下列叙述正确的是( )
| A. | 原子核都由质子和中子构成 | |
| B. | 在原子中,核内的质子数与核外的电子数不一定相等 | |
| C. | 原子里有相对很大的空间,电子在这个空间里作高速运动 | |
| D. | 不同种类的原子,核内的质子数不同,核外电子数可以不等于质子数 |
8.胃酸过多的人不能服用( )
| A. | 小苏打 | B. | 氢氧化铝 | C. | 消石灰 | D. | 珍珠粉 |
5.用灯帽熄灭酒精灯,该灭火方法的主要原理是( )
| A. | 清除可燃物 | B. | 降低可燃物着火点 | ||
| C. | 隔绝氧气 | D. | 使可燃物的温度降到着火点以下 |