题目内容
19.下列有关溶液的说法错误的是( )| A. | 溶液一定是无色透明的 | B. | 一种溶液中溶质可以有多种 | ||
| C. | 溶质可以是固体、液体或气体 | D. | 稀溶液也可能是饱和溶液 |
分析 A、溶液可以有颜色;B、根据溶液中溶质的种类考虑;C、根据溶质的状态考虑;D、根据溶液浓稀和是否饱和的关系考虑.
解答 解:A、溶液可以有颜色,例如硫酸铜溶液是蓝色,故A说法错误;
B、溶液中溶质可以有一种或多种,故B说法正确;
C、溶质可以是固体例如氯化钠溶液、可以是液体例如酒精溶液或可以是气体例如汽水,故C说法正确;
D、溶液浓稀和是否饱和没有关系,饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液,故D说法正确.
故选A.
点评 解答本题关键是熟悉溶液的特点、组成,知道溶质的种类.

练习册系列答案
相关题目
9. 如图,广口瓶中盛有气体X,胶头滴管中盛有液体Y.若挤压胶头滴管使液体滴入瓶中,振荡,一段时间后可见小气球a膨胀鼓起.下列各组物质不会出现上述现象的是( )
如图,广口瓶中盛有气体X,胶头滴管中盛有液体Y.若挤压胶头滴管使液体滴入瓶中,振荡,一段时间后可见小气球a膨胀鼓起.下列各组物质不会出现上述现象的是( )
 如图,广口瓶中盛有气体X,胶头滴管中盛有液体Y.若挤压胶头滴管使液体滴入瓶中,振荡,一段时间后可见小气球a膨胀鼓起.下列各组物质不会出现上述现象的是( )
如图,广口瓶中盛有气体X,胶头滴管中盛有液体Y.若挤压胶头滴管使液体滴入瓶中,振荡,一段时间后可见小气球a膨胀鼓起.下列各组物质不会出现上述现象的是( )| X | Y | |
| A | HCl | Ca(OH)2 |
| B | CO2 | NaOH |
| C | CO | Ba(OH)2 |
| D | SO2 | KOH |
| A. | A | B. | B | C. | C | D. | D |
10.某学生在课外活动中用一定量的二价金属R和稀硫酸反应来制取氢气,所做5次实验结果记录如下表(假设每次实验所产生的氢气全部被收集,体积在同温同压下测定).
根据上述实验结果进行分析、计算,并回答下列问题:
(1)实验3中,金属R是否过量?(填“过量”、“不足”、“恰好反应”)恰好反应,其判断依据是数据可以看出,酸的量一定,反应中酸过量时,金属质量和氢气的量成正比,酸不足时,氢气的量不再发生变化,$\frac{1.5}{1.47}=\frac{2.0}{1.96}=\frac{2.2}{2.16}$,实验4和5气体体积不变,则实验3可认为是恰好反应.
(2)若在当时实验条件下,H2的密度为0.085g/L,使用的稀硫酸密度为1.12g/cm3,则实验1所得溶液中RSO4的质量分数为13.1%.
(3)t℃时,若实验3所得RSO4溶液恰好构成饱和溶液,则该温度下RSO4的溶解度是24.4g.
| 实验编号 | R的质量/g | 稀硫酸的体积/mL | 生成H2的体积/L |
| 1 | 1.5 | 50.0 | 1.47 |
| 2 | 2.0 | 50.0 | 1.96 |
| 3 | 2.2 | 50.0 | 2.16 |
| 4 | 2.5 | 50.0 | 2.16 |
| 5 | 3.0 | 50.0 | 2.16 |
(1)实验3中,金属R是否过量?(填“过量”、“不足”、“恰好反应”)恰好反应,其判断依据是数据可以看出,酸的量一定,反应中酸过量时,金属质量和氢气的量成正比,酸不足时,氢气的量不再发生变化,$\frac{1.5}{1.47}=\frac{2.0}{1.96}=\frac{2.2}{2.16}$,实验4和5气体体积不变,则实验3可认为是恰好反应.
(2)若在当时实验条件下,H2的密度为0.085g/L,使用的稀硫酸密度为1.12g/cm3,则实验1所得溶液中RSO4的质量分数为13.1%.
(3)t℃时,若实验3所得RSO4溶液恰好构成饱和溶液,则该温度下RSO4的溶解度是24.4g.
7. PX化学名称为对二甲苯.其主要性质有:无色透明液体,具有芳香气味,能与乙醇等有机溶剂混溶,可燃,低毒,毒性略高于乙醇,其蒸气与空气可形成爆炸性混合物.右图是“PX”的结构模型,下列有关“PX”的说法不正确的是( )
PX化学名称为对二甲苯.其主要性质有:无色透明液体,具有芳香气味,能与乙醇等有机溶剂混溶,可燃,低毒,毒性略高于乙醇,其蒸气与空气可形成爆炸性混合物.右图是“PX”的结构模型,下列有关“PX”的说法不正确的是( )
 PX化学名称为对二甲苯.其主要性质有:无色透明液体,具有芳香气味,能与乙醇等有机溶剂混溶,可燃,低毒,毒性略高于乙醇,其蒸气与空气可形成爆炸性混合物.右图是“PX”的结构模型,下列有关“PX”的说法不正确的是( )
PX化学名称为对二甲苯.其主要性质有:无色透明液体,具有芳香气味,能与乙醇等有机溶剂混溶,可燃,低毒,毒性略高于乙醇,其蒸气与空气可形成爆炸性混合物.右图是“PX”的结构模型,下列有关“PX”的说法不正确的是( )| A. | “PX”属于有机化合物 | |
| B. | “PX”可燃,具有芳香气味,低毒都属于它的化学性质 | |
| C. | “PX”中C、H两种元素的质量比为48:5 | |
| D. | “PX”的化学式为C8H10 |
4.下列物质的用途,利用了物理性质的是( )
| A. | 用稀硫酸除铁锈 | B. | 氢气做燃料 | ||
| C. | 用熟石灰改良酸性土壤 | D. | 干冰用于人工降雨 |
 根据如图所示二氧化碳和氧气的性质实验,请回答以下问题.
根据如图所示二氧化碳和氧气的性质实验,请回答以下问题.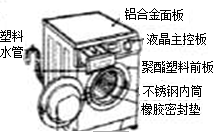 洗衣机是生活中家庭常用的必需品,如图所示是某品牌洗衣机图,请回答下列问题.
洗衣机是生活中家庭常用的必需品,如图所示是某品牌洗衣机图,请回答下列问题. 如图所示A~G是初中化学中常见的物质(反应条件和部分产物已省略,“-”表示相互能反应,“→”表示转化关系),其中A是人体胃液中含有的酸,B与C的组成元素相同,D是一种红色粉末,F是相对分子质量最小的氧化物.请回答下列问题.
如图所示A~G是初中化学中常见的物质(反应条件和部分产物已省略,“-”表示相互能反应,“→”表示转化关系),其中A是人体胃液中含有的酸,B与C的组成元素相同,D是一种红色粉末,F是相对分子质量最小的氧化物.请回答下列问题.