题目内容
某化学活动小组需要用溶质质量分数为19.6%的稀硫酸和锌粒反应来制取氢气,但实验室现有的是溶质质量分数为98%的浓硫酸。试计算:
(1)将10g浓硫酸配制成所需的稀硫酸,需要水的质量为多少?
(2)取上述配制好的稀硫酸20g与足量锌粒充分反应,能制得氢气质量为多少?
(反应的化学方程式为Zn+H2SO4 = ZnSO4+H2↑)
【答案】
(1)解:设加水后溶液的质量为x
10g ×98%= x×19.6% (1分)
x =50g (1分)
需要水的质量=50g一l0g =40g (1分)
(2)解:设生成氢气的质量为x
Zn+H2SO4=ZnSO4 + H2↑ (1分)
98 2
20g×19.6% x (1分)
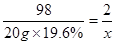 (1分)
(1分)
x =0. 08g (2分)
【解析】
试题分析:(1)溶液稀释的计算根据稀释前后溶液中溶质的质量不变列式;先计算出稀释后溶液的质量,再用溶液的质量减去稀释前溶液的质量;(2)先计算出20g49.6%的硫酸中硫酸的质量,再利用化学方程式,可求出氢气的质量。
考点:溶液的计算、化学方程式的计算

练习册系列答案
相关题目