题目内容
 小莹同学的父亲买回一袋钾肥,其包装袋上的部分内容如图所示.为了确定该化肥的纯度是否符合标准,小莹同学称取10g样品,加入适量的水溶解后与足量的BaCl2溶液充分反应,经过过滤、洗涤、烘干沉淀,测得其质量为11.65g.试通过计算确定该化肥纯度是否符合包装袋上的说明.(K2SO4+BaCl2═BaSO4↓+2KCl,假设化肥中的杂质不与BaCl2溶液反应.)提示:纯度即样品中硫酸钾的质量分数.
小莹同学的父亲买回一袋钾肥,其包装袋上的部分内容如图所示.为了确定该化肥的纯度是否符合标准,小莹同学称取10g样品,加入适量的水溶解后与足量的BaCl2溶液充分反应,经过过滤、洗涤、烘干沉淀,测得其质量为11.65g.试通过计算确定该化肥纯度是否符合包装袋上的说明.(K2SO4+BaCl2═BaSO4↓+2KCl,假设化肥中的杂质不与BaCl2溶液反应.)提示:纯度即样品中硫酸钾的质量分数.考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:为确定该化肥纯度是否符合包装袋上的说明,需要计算10g样品中K2SO4的质量分数;10g样品中K2SO4的质量分数=
×100%,其中样品中硫酸钾的质量可通过反应的化学方程式,由生成沉淀硫酸钡的质量11.65g计算出来.
| 样品中硫酸钾的质量 |
| 样品质量 |
解答:解:设10g化肥样品中含K2SO4的质量为x
K2SO4+BaCl2=BaSO4↓+2KCl
174 233
x 11.65g
=
x=8.7g
硫酸钾的质量分数(纯度)=
×100%=87%<95%
答:该化肥的纯度不符合包装袋上的说明.
K2SO4+BaCl2=BaSO4↓+2KCl
174 233
x 11.65g
| 174 |
| 233 |
| x |
| 11.65g |
x=8.7g
硫酸钾的质量分数(纯度)=
| 8.7g |
| 10g |
答:该化肥的纯度不符合包装袋上的说明.
点评:根据反应的化学方程式可以表示反应中各物质的质量关系,由反应中某物质的质量可计算出反应中其它物质的质量.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
某收藏爱好者收藏了一件清末的铝制佛像,而该佛像至今仍保存十分完好,该佛像不易锈蚀的原因是( )
| A、铝不易发生化学反应 |
| B、铝易氧化,但氧化铝具有保护内部铝的作用 |
| C、铝不易氧化 |
| D、铝的氧化物易发生还原反应 |
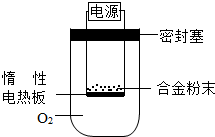 镁合金的强度高、机械性能好.这些特性使金属镁成为制造汽车、飞机、火箭的重要材料,从而获得“国防金属”的美誉.为测定约含镁30%的镁铝合金(不含其他元素)中镁的质量分数.
镁合金的强度高、机械性能好.这些特性使金属镁成为制造汽车、飞机、火箭的重要材料,从而获得“国防金属”的美誉.为测定约含镁30%的镁铝合金(不含其他元素)中镁的质量分数.