题目内容
1.某温度下,向一定量的饱和石灰水中加入少量的生石灰,恢复到原来的温度.此时( )| A. | 溶液的质量不变 | B. | 溶液的质量变小 | ||
| C. | 溶液中溶质的质量分数增大 | D. | 溶质的溶解度增大 |
分析 根据某温度时,向一定量的饱和石灰水中加入少量的生石灰,恢复到原来的温度,因此不需要考虑温度对溶液的影响;生石灰与水发生反应生成氢氧化钙,反应消耗了饱和溶液中的水,而使饱和溶液因减少溶剂水,而析出固体,饱和溶液中的溶质、溶剂质量减少,溶液仍为该温度下的饱和溶液,据此进行分析解答.
解答 解:A、氧化钙会与水反应,溶剂质量减少,溶质质量减少,所以溶液质量减少,故A错误;
B、氧化钙会与水反应,溶剂质量减少,溶质质量减少,所以溶液质量减少,故B正确;
C、氧化钙会与水反应,溶液质量减少,仍然是该温度下的饱和溶液,所以溶质质量分数不变,故C错误;
D、温度不变,溶解度不变,故D错误.
故选:B.
点评 本题难度不大,掌握生石灰与水的反应、反应后溶液组成的变化是正确解答本题的关键.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
12.小丽为探究分子的运动速率与温度的关系:取等量的品红分别加入到等量的热水和冷水中,观察并记录实验现象在表中:
根据实验现象,可得出结论:温度升高,分子能量增大,运动速率加大.
| 实验过程 | 冷水 | 热水 |
| 开始 | 红色扩散较慢 | 红色扩散很快 |
| 长久放置 | 最终均成为红色、均匀、透明的液体 | |
16.某同学在家里自制紫甘蓝汁,发现其性质稳定,分别滴加到下列不同的试剂中,并记录观察到的现象如表所示,分析下列表格信息问答:
(1)该种自制指示剂与石蕊溶液(填“石蕊溶液”或“酚酞溶液”)变色原理相似.
(2)正常雨水经测定其pH略显酸性,其原因用化学方程式说明:CO2+H2O═H2CO3.
(3)在厨房清洁剂中加入蒸馏水,其碱性会减弱(填“增强”或“减弱”).
(4)厨房清洁剂与厕所清洁剂不能混合使用,其原因是二者会发生中和反应.
| 试剂 | 厕所清洁剂 (含盐酸) | 正常雨水 | 蒸馏水 | 糖水 | 厨房清洁剂 (含氢氧化钠) | 石灰水 |
| 颜色 | 红 | 红 | 黄 | 绿 | 绿 | 绿 |
(2)正常雨水经测定其pH略显酸性,其原因用化学方程式说明:CO2+H2O═H2CO3.
(3)在厨房清洁剂中加入蒸馏水,其碱性会减弱(填“增强”或“减弱”).
(4)厨房清洁剂与厕所清洁剂不能混合使用,其原因是二者会发生中和反应.
6.很多化学反应都在溶液里进行的原因是( )
| A. | 反应物粒子容易接触碰撞,使反应进行得快 | |
| B. | 固体物质不能直接反应 | |
| C. | 设备简单 | |
| D. | 可以不进行加热 |
13.化学实验技能是学习化学和进行探究活动的基础和保证.以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究:
【提出问题】化学反应前后各物质的质量总和是否相等?
【猜想与假设】猜想1:不相等; 猜想2:相等.
【实验探究】甲、乙两组同学用托盘天平分别称量反应前后物质的质量.
【反思评价】究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转.得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在密闭容器中进行.
【优化装置】同学们对甲组左盘中的反应装置进行了如下三种改进,查阅资料后发现最佳装置是B,则猜想B中氢氧化钠具有的化学性质是能与二氧化碳发生反应.

【得出结论】同学们利用改进后的最佳装置进行再次探究,均得出猜想2正确.进一步分析发现,反应体系中器材和未参加反应的物质的质量在反应前后保持不变,最终得出结论:参加化学反应(或参加反应)的各物质的质量总和等于反应后生成的各物质的质量总和.
【解释应用】解释:化学反应前后,原子的种类、数目、质量均不变,所以质量守恒.
应用:硝酸铵(NH4NO3)固体在不同温度下发生不同的分解反应,则下列各物质可能是该反应产物的是ABD(填序号).
A.NH3 B.H2O C.SO2D.N2.
【提出问题】化学反应前后各物质的质量总和是否相等?
【猜想与假设】猜想1:不相等; 猜想2:相等.
【实验探究】甲、乙两组同学用托盘天平分别称量反应前后物质的质量.
| 甲 组 | 乙 组 | |
| 实验 方案 (反应后略) | 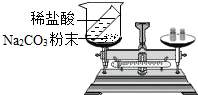 | 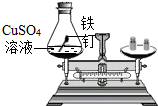 |
| 实验 现象 | 有气泡产生, 天平指针向右偏转 | 铁钉表面有红色物质析出, 溶液颜色发生改变, 天平指针没有偏转 |
| 结论 | 猜想1正确 | 猜想2正确 反应的化学方程式:Fe+CuSO4=FeSO4+Cu |
【优化装置】同学们对甲组左盘中的反应装置进行了如下三种改进,查阅资料后发现最佳装置是B,则猜想B中氢氧化钠具有的化学性质是能与二氧化碳发生反应.

【得出结论】同学们利用改进后的最佳装置进行再次探究,均得出猜想2正确.进一步分析发现,反应体系中器材和未参加反应的物质的质量在反应前后保持不变,最终得出结论:参加化学反应(或参加反应)的各物质的质量总和等于反应后生成的各物质的质量总和.
【解释应用】解释:化学反应前后,原子的种类、数目、质量均不变,所以质量守恒.
应用:硝酸铵(NH4NO3)固体在不同温度下发生不同的分解反应,则下列各物质可能是该反应产物的是ABD(填序号).
A.NH3 B.H2O C.SO2D.N2.
10.下列根据实验目的所设计的实验方案正确的是( )
| 选项 | 实验目的 | 实验设计 |
| A | 除去CO2中的CO | 点燃 |
| B | 测定某地雨水是否为酸雨 | 加紫色石蕊,观察颜色变化 |
| C | 检验氢氧化钠溶液是否变质 | 加无色酚酞,观察颜色变化 |
| D | 探究燃烧的条件之一是需要可燃物 | 用棉花分别蘸酒精和水,放在酒精灯火焰上加热片刻,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
11.正确的实验操作是进行科学实验的重要保障,下列实验操作中合理的是( )
| A. | 测定某溶液pH时,先将pH试纸润湿 | |
| B. | 用漏斗过滤时,可用玻璃棒搅拌以加快过滤速度 | |
| C. | 少量酒精在实验台上燃烧时,立即用湿抹布盖灭 | |
| D. | 氢氧化钠不慎沾到皮肤上时,应先用水冲洗,再涂3-5%小苏溶液 |
