题目内容
用一氧化碳还原氧化铜的方法制取铜.若要得到128克铜,需要氧化铜多少?同时放出二氧化碳多少?在标准状况下33.6升的一氧化碳和足量的氧化铜反应,可得到多少克铜?(ρco=1.25克/升)
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:一氧化碳在加热条件下还原氧化铜生成铜和二氧化碳,利用该反应的化学方程式确定反应生成铜与氧化铜、二氧化碳的质量关系,由生成铜的质量则可完成氧化铜、二氧化碳的质量的计算;
利用二氧化碳的体积算出二氧化碳的质量,根据二氧化碳的质量求铜的质量.
利用二氧化碳的体积算出二氧化碳的质量,根据二氧化碳的质量求铜的质量.
解答:解:设需要氧化铜的质量为x,放出二氧化碳的质量为y
CuO+CO
Cu+CO2
80 64 44
x 128g y
=
=
x=160g,y=88g
一氧化碳的质量为:33.6升×1.25克/升=42克
设得到铜的质量为z
CuO+CO
Cu+CO2
28 64
42g z
=
z=96g
答:若要得到128克铜,需要氧化铜的质量为160g,放出二氧化碳88g;在标准状况下33.6升的一氧化碳和足量的氧化铜反应,可得到96g铜.
CuO+CO
| ||
80 64 44
x 128g y
| 80 |
| x |
| 64 |
| 128g |
| 44 |
| y |
x=160g,y=88g
一氧化碳的质量为:33.6升×1.25克/升=42克
设得到铜的质量为z
CuO+CO
| ||
28 64
42g z
| 28 |
| 64 |
| 42g |
| z |
z=96g
答:若要得到128克铜,需要氧化铜的质量为160g,放出二氧化碳88g;在标准状况下33.6升的一氧化碳和足量的氧化铜反应,可得到96g铜.
点评:化学方程式可以表示反应中各物质的质量关系,利用反应中任一物质的质量可计算反应中其它物质的质量.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
有关物理量相应的单位表达错误的是( )
| A、摩尔质量g/mol |
| B、气体体积L/mol |
| C、溶解度g/100g |
| D、密度g/cm3 |
 如图是“电解水实验”的装置图,根据所学知识回答问题:
如图是“电解水实验”的装置图,根据所学知识回答问题: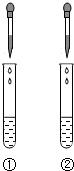 小李在化学实验技能考查中,完成“【实验一】小李取待测液甲、乙分别放置在试管①和②,再往两支试管中滴入稀盐酸,观察实验现象.根据现象推知,乙为碳酸钠溶液.
小李在化学实验技能考查中,完成“【实验一】小李取待测液甲、乙分别放置在试管①和②,再往两支试管中滴入稀盐酸,观察实验现象.根据现象推知,乙为碳酸钠溶液. A、B、C、D为初中常见的物质,相互之间的关系如图所示(“-”表示两种物质间能发生反应,“→”表示两种物质间能够转化,部分反应物或生成物以及反应条件已略去).
A、B、C、D为初中常见的物质,相互之间的关系如图所示(“-”表示两种物质间能发生反应,“→”表示两种物质间能够转化,部分反应物或生成物以及反应条件已略去).