题目内容
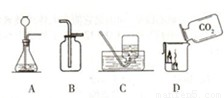
某化学兴趣小组的同学,设计了如下实验:二氧化碳制取和性质的探究.请回答有关问题:(1)实验室制取二氧化碳时,应选用的发生装置和收集装置是 (填写装置的字母代号),请写出该反应的化学方程式: .
(2)如图D所示,向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳具有的性质是 .
【答案】分析:(1)实验室制取二氧化碳用稀盐酸和大理石或石灰石反应,适合固液常温型反应装置;二氧化碳能溶于水且能和水反应,故只能用向上排空气法收集.
(2)根据二氧化碳的化学性质、物理性质进行分析解答.
解答:解:(1)实验室制取二氧化碳用稀盐酸和大理石或石灰石反应,适合固液常温型反应装置;二氧化碳能溶于水且能和水反应,故只能用向上排空气法收集;则应选用的发生装置和收集装置分别是A、B.反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O.
(2)向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳不能燃烧、不能支持燃烧,二氧化碳比空气密度大.
故答案为:(1)A、B;CaCO3+2HCl=CaCl2+CO2↑+H2O;(2)不能燃烧、不能支持燃烧,二氧化碳比空气密度大.
点评:本题难度不大,掌握二氧化碳的实验室制法、二氧化碳的化学性质与物理性质是正确解答本题的关键.
(2)根据二氧化碳的化学性质、物理性质进行分析解答.
解答:解:(1)实验室制取二氧化碳用稀盐酸和大理石或石灰石反应,适合固液常温型反应装置;二氧化碳能溶于水且能和水反应,故只能用向上排空气法收集;则应选用的发生装置和收集装置分别是A、B.反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O.
(2)向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳不能燃烧、不能支持燃烧,二氧化碳比空气密度大.
故答案为:(1)A、B;CaCO3+2HCl=CaCl2+CO2↑+H2O;(2)不能燃烧、不能支持燃烧,二氧化碳比空气密度大.
点评:本题难度不大,掌握二氧化碳的实验室制法、二氧化碳的化学性质与物理性质是正确解答本题的关键.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
 12、碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.
12、碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.


 (2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.
(2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹. 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.