题目内容
11.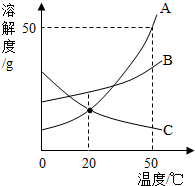 如图所示是A、B、C三种物质的溶解度曲线,下列分析正确的是( )
如图所示是A、B、C三种物质的溶解度曲线,下列分析正确的是( )| A. | 20℃时,三种物质的溶解度由大到小的顺序是B>A>C | |
| B. | 50℃时,A的饱和溶液的溶质质量分数是50% | |
| C. | 将20℃时三种物质的饱和溶液升高到50℃时,得到的都是饱和溶液 | |
| D. | 将50℃时100gA、B、C三种物质的饱和溶液降温到20℃,析出固体A最多 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、通过分析溶解度曲线可知,20℃时,三种物质的溶解度由大到小的顺序是B>A=C,故A错误;
B、50℃时,A物质的溶解度是50g,所以A的饱和溶液的溶质质量分数是33.3%,故B错误;
C、A、B物质的溶解度随温度的升高而增大,所以将20℃时三种物质的饱和溶液升高到50℃时,A、B物质不能达到饱和溶液,故C错误;
D、A物质的溶解度受温度影响变化最大,所以将50℃时100gA、B、C三种物质的饱和溶液降温到20℃,析出固体A最多,故D正确.
故选:D.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
2.将酚酞试液滴入碳酸钠溶液中,发现溶液变成了红色.由此可得到的信息是( )
| A. | 碳酸钠是一种碱 | B. | 碳酸钠溶液呈碱性 | ||
| C. | 碳酸钠是一种白色固体 | D. | 碳酸钠的化学式为Na2CO3 |
6.物质的性质决定物质的用途.下列物质的用途中,利用其化学性质是( )
①氮气作保护气②铝用作导线③生石灰作干燥剂④小苏打用于焙制糕点⑤洗涤剂用于除油污.
①氮气作保护气②铝用作导线③生石灰作干燥剂④小苏打用于焙制糕点⑤洗涤剂用于除油污.
| A. | ①②③ | B. | ①④⑤ | C. | ①③④ | D. | ②③⑤ |
3.化学实验涉及到很多物质的检验,下列检验中,错误的是( )
| A. |  检验装置气密性 | B. | 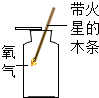 验满氧气 | C. | 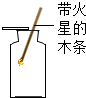 检验二氧化碳 | D. |  氢气验纯 |
20.分类法是化学学习的常用方法.下列分类中正确的是( )
| A. | 混合物:空气、溶液、冰水共存物 | B. | 合成材料:塑料、橡胶、合金 | ||
| C. | 人体必需微量元素:铁、锌、钠 | D. | 有机化合物:甲烷、乙醇、乙酸 |
1.如表是氯化钠和硝酸钾在不同温度时的溶解度,根据此表回答
(1)60℃时,氯化钠的溶解度为37.3g.
(2)在30℃时,100g水中加入50g硝酸钾,充分搅拌后得到的溶液质量为145.8g.
(3)欲从海水中获得氯化钠晶体,应采取蒸发溶剂方法.
(4)由表中数据分析可知,硝酸钾和氯化钠在某一温度时具有相同的溶解度x,则x的取值范围是36.0<x<36.3g.
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
(2)在30℃时,100g水中加入50g硝酸钾,充分搅拌后得到的溶液质量为145.8g.
(3)欲从海水中获得氯化钠晶体,应采取蒸发溶剂方法.
(4)由表中数据分析可知,硝酸钾和氯化钠在某一温度时具有相同的溶解度x,则x的取值范围是36.0<x<36.3g.