题目内容
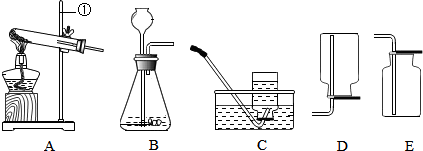
19.根据如图所示装置回答下列有关问题:
(1)写出标号仪器的名称a长颈漏斗.
(2)用高锰酸钾制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,可选择的发生装置是A(填字母).
(3)实验室制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,可选择的收集装置是D(填字母).
(4)①实验室若要配制5%的双氧水150g,需要30%双氧水(密度1.1g/cm3)22.7ml.(结果保留一位小数)
②某同学取68g上述配制好的双氧水用于实验室制氧气,理论上最多可产生氧气的质量多少?(写出计算过程)1.6g.
分析 (1)熟记仪器的名称;
(2)根据高锰酸钾制取氧气的原理正确书写出化学方程式,发生装置选择加热固体产生气体的A装置;
(3)实验室通常用大理石或石灰石和稀盐酸反应生成氯化钙、水和二氧化碳;二氧化碳能够溶于水,密度比空气大;
(4)稀释浓溶液时,可根据溶质质量不变列等式算出双氧水质量;结合化学方程式进行计算即可.
解答 解:(1)仪器a是长颈漏斗;故填:长颈漏斗;
(2)用高锰酸钾制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,发生装置选择加热固体产生气体的A装置;故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;A;
(3)实验室制取二氧化碳的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;因为二氧化碳能够溶于水,密度比空气大,故选择的收集装置是D.故填:CaCO3+2HCl=CaCl2+H2O+CO2↑;D;
(4)①设需要30%的双氧水的质量为x:由150g×5%=x×30%,解得x=25g;故需要30%双氧水(密度1.1g/cm3):$\frac{25g}{1.1g/mL}$≈22.7mL.
②解:设理论上最多可产生氧气质量为x.
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
68g×5% x
$\frac{68}{32}=\frac{68g×5%}{x}$
解得x=1.6g.
故答案为:
①22.7;
②解:设理论上最多可产生氧气质量为x.
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
68g×5% x
$\frac{68}{32}=\frac{68g×5%}{x}$
解得x=1.6g.
点评 本考点主要考查气体的制取装置和收集装置的选择、仪器的名称,同时也考查了化学方程式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 铜能导电 | B. | 氢氧化钙微溶于水 | ||
| C. | 镁能与氧气反应 | D. | 常温下甲烷是无色无味气体 |
| A. | 干冰用于人工降雨 | B. | 小苏打用于治疗胃酸过多 | ||
| C. | 硫酸用于金属除锈 | D. | 熟石灰用于改良酸性土壤 |
 甲、乙、丙、丁是初中化学常见的物质,常温下,它们具有如图所示关系,“-”表示连接的两种物质能反应,“→”表示物质转化的方向,下列推断错误的是( )
甲、乙、丙、丁是初中化学常见的物质,常温下,它们具有如图所示关系,“-”表示连接的两种物质能反应,“→”表示物质转化的方向,下列推断错误的是( )| A. | 若甲是HCl,则丁可能是CuCl2 | |
| B. | 若甲是H2SO4,则乙和丙中可能有一种为单质 | |
| C. | 若甲是Ca(OH)2,则丁可能是KOH | |
| D. | 若甲是Ca(OH)2,丁是NaOH,则乙和丙中必须有一种为酸 |
| A. | 空气是一种化合物--含有多种分子 | |
| B. | 氢气和液氧的化学性质相同--两者的分子构成相同 | |
| C. | 盛有香水的瓶子敞口久置后香水“消失--分子在不断运动 | |
| D. | 化学反应前后物质总质量不变--反应前后分子的种类和个数都不变 |
 下列实验符合如图所示变化趋势的是( )
下列实验符合如图所示变化趋势的是( )| 序号 | 实验 | 横坐标 | 纵坐标 |
| A | 向一定量氢氧化钠溶液中滴加稀硫酸 | 稀硫酸的质量 | 水的质量 |
| B | 加热一定量高锰酸钾固体 | 时间 | 剩余固体中氧元素的质量 |
| C | 向一定量饱和硝酸钾溶液中加水 | 加水的质量 | 溶质的质量分数 |
| D | 向一定量镁粉中加入稀盐酸 | 稀盐酸的质量 | 镁粉的质量 |
| A. | A | B. | B | C. | C | D. | D |
 如图为水电解器结构示意图.
如图为水电解器结构示意图.