题目内容
10.下列各物质按照混合物、单质、氧化物的顺序排列的是( )| A. | 水银、冰、医用消毒酒精 | B. | 溴、熟石灰、盐酸 | ||
| C. | 石墨、石灰石、醋酸 | D. | 空气、氮气、二氧化碳 |
分析 题考查利用单质、氧化物、混合物的概念来判断物质类别,由一种元素组成的纯净物是单质,由两种元素组成且一种是氧元素的化合物属于氧化物,由不同物质组成的物质属于混合物
解答 解:A、水银属于单质、冰属于氧化物、医用消毒酒精属于混合物,故A错;
B、溴属于单质、熟石灰属于化合物、盐酸属于混合物,故B错;
C、石墨属于单质、石灰石属于混合物、醋酸属于混合物,故C错;
D、空气属于混合物、氮气属于单质、二氧化碳属于氧化物,故D正确.
故选D.
点评 应抓住概念的要点来判断物质的类别,了解常见物质的组成.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
20.下列实验操作、现象与结论对应关系正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向醋酸中加入氢氧化钠溶液 | 无明显现象 | 二者之间不发生反应 |
| B | 向样品溶液中先滴加BaCl2溶液,再滴加过量的稀硝酸 | 滴加BaCl2后出现白色沉淀,再滴加稀硝酸沉淀不消失 | 样品溶液中含有SO42- |
| C | 将两根铁丝分别伸入硫酸铜溶液和硝酸银溶液中 | 两个铁丝上均有固体附着 | 金属的活动性顺序为Fe>Cu>Ag |
| D | 用导管分别对准浸没在热水和冷水中的白磷通入氧气 | 热水中的白磷燃烧,冷水中的白磷不燃烧 | 燃烧的条件之一是温度达到着火点 |
| A. | A | B. | B | C. | C | D. | D |
1.青铜是铜锡合金.我国古代金属锡的冶炼发生的反应主要是:SnO2+2C$\frac{\underline{\;高温\;}}{\;}$Sn+2CO↑,该反应类型属于( )
| A. | 化合反应 | B. | 分解反应 | C. | 复分解反应 | D. | 置换反应 |
15.小明买了一种“汽泡爽”的冲调饮料(如图1).

(1)小明阅读资料发现:“汽泡爽”原料中的柠檬酸和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,请填写柠檬酸的化学式.3NaHCO3+C6H8O7═C6H5O7Na3+3H2O+3CO2↑
(2)小明想探究加水温度对产生气体量的影响,小明设计了如下实验方案.
在老师的帮助下,小明采用相同的两套实验装置(如图2)分别完成上述实验,在A中加入水,再加入一袋“汽泡爽”,迅速塞紧胶塞.量筒C用于收集A中产生的气体所排出的液体,冷却至室温后读取数据.B中油层的作用是防止二氧化碳溶于水.
(3)通过实验,小明测得:a=64mL,b=132mL,由此获得结论:“汽泡爽”产生气体的量与加水温度有关系.但是老师看到小明的实验报告后却指出:两套装置中,“汽泡爽”产生气体的总量应该近似相等,与温度关系不大,其本质原因是反应物的量不变生成物的量也不变.
(4)通过反思,为了证明老师的观点,小明继续利用(3)中已反应完的两套装置,又做了一步实验,发现两套装置最终收集到的气体的总量确实相近,他的实验操作是不断摇动两套装置中的锥形瓶A,继续收集气体并测量体积.

(1)小明阅读资料发现:“汽泡爽”原料中的柠檬酸和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,请填写柠檬酸的化学式.3NaHCO3+C6H8O7═C6H5O7Na3+3H2O+3CO2↑
(2)小明想探究加水温度对产生气体量的影响,小明设计了如下实验方案.
| 实验序号 | 加入水的体积 | 加入水的温度 | 收集到的气体的体积 |
| 1 | 200mL | 15℃ | a(待记录) |
| 2 | 200mL | 50℃ | b(待记录) |
(3)通过实验,小明测得:a=64mL,b=132mL,由此获得结论:“汽泡爽”产生气体的量与加水温度有关系.但是老师看到小明的实验报告后却指出:两套装置中,“汽泡爽”产生气体的总量应该近似相等,与温度关系不大,其本质原因是反应物的量不变生成物的量也不变.
(4)通过反思,为了证明老师的观点,小明继续利用(3)中已反应完的两套装置,又做了一步实验,发现两套装置最终收集到的气体的总量确实相近,他的实验操作是不断摇动两套装置中的锥形瓶A,继续收集气体并测量体积.
2.下列名称与化学符号一致的是( )
| A. | Na2CO3 小苏打 | B. | CO 一氧化碳 | ||
| C. | NH4 氨气 | D. | CO32- 碳酸根离子 |
19. 次氯酸钠溶液,俗称漂白水,在烧碱溶液中通入氯气即可制得.漂白水为无色或淡黄绿色液体,
次氯酸钠溶液,俗称漂白水,在烧碱溶液中通入氯气即可制得.漂白水为无色或淡黄绿色液体,
可与水无限比例混溶,遇热、遇光易分解;在碱性环境下,杀菌效果很差;常用于对饮用水和废
水进行杀菌处理.【光照强度:阳光直射的夏季约为6万-10万lx(勒克斯),夏天明朗的室内约为100-550k】
为探究哪些因素对杀菌速率的影响,某兴趣小组实验如下:
(1)控制细菌初始浓度相同,实验温度恒定在25℃或10℃,完成以下实验设计表(表中不要留空格).
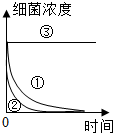
实验测得细菌浓度随时间变化的关系如图.
(2)实验①、②表明温度升高,杀菌速率下降.
(3)在碱性环境下,杀菌效果很差的可能原因是次氯酸钠分解了.
 次氯酸钠溶液,俗称漂白水,在烧碱溶液中通入氯气即可制得.漂白水为无色或淡黄绿色液体,
次氯酸钠溶液,俗称漂白水,在烧碱溶液中通入氯气即可制得.漂白水为无色或淡黄绿色液体,可与水无限比例混溶,遇热、遇光易分解;在碱性环境下,杀菌效果很差;常用于对饮用水和废
水进行杀菌处理.【光照强度:阳光直射的夏季约为6万-10万lx(勒克斯),夏天明朗的室内约为100-550k】
为探究哪些因素对杀菌速率的影响,某兴趣小组实验如下:
(1)控制细菌初始浓度相同,实验温度恒定在25℃或10℃,完成以下实验设计表(表中不要留空格).
| 编号 | 实验目的 | 温度/℃ | pH | 光照/lx |
| ① | 为②③提供对照 | 25 | 5 | 300 |
| ② | 探究温度对杀菌速率的影响 | 10 | 5 | 300 |
| ③ | 探究光强对杀菌速率的影响 | 10 | 5 | 80000 |
(2)实验①、②表明温度升高,杀菌速率下降.
(3)在碱性环境下,杀菌效果很差的可能原因是次氯酸钠分解了.
16.下列物质中前者是混合物后者是单质的是( )
| A. | 石灰水,二氧化碳 | B. | 冰水混合物,氦气 | C. | 高锰酸钾,硫磺 | D. | 洁净的空气,汞 |