题目内容
 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:(1)t2℃时,80g a物质加入到150g水中不断搅拌,充分溶解后形成的溶液质量是
(2)P点的含义是
(3)t2℃时,等质量的a、b、c的饱和溶液,冷却到t1℃,析出晶体最多的是
(4)N点所示的c溶液为某温度下c的
(5)将t1℃时,a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是
(6)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为a、b、c三种固体物质中的哪一种?
考点:固体溶解度曲线及其作用,饱和溶液和不饱和溶液相互转变的方法,晶体和结晶的概念与现象,用水稀释改变浓度的方法,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:根据固体的溶解度曲线可以:①比较不同物质在同一温度下的溶解度大小,②判断出物质的溶解度随温度变化的变化情况,从而确定通过降温还是升温的方式使溶质从溶液中结晶析出.
解答:解:(1)t2℃时,a物质的溶解度是50g,80g a物质加入到150g水中不断搅拌,只能溶解a物质的质量是75g,充分溶解后形成的溶液质量是150g+75g=225g,故填:225;
(2)P点时a和c的溶解度相交,表示在t1℃时ac的溶解度相等;该温度下a物质的溶解度是20g,若将a物质溶液恒温蒸发20g水,会有a晶体
×20g=4g析出.满足P点指标的a物质溶液120g,若需溶质质量分数减小为原来的一半,则溶质质量不变,设加水的质量为x,则有(120g+x)×
×
=20g,解得x=120g;故填:t1℃时ac的溶解度相等,4,120;
(3)t2℃时,a的溶解度受温度影响变化大,等质量的a、b、c的饱和溶液,冷却到t1℃,析出晶体最多的是a,c的溶解度随温度的降低而正大,没有晶体析出,故填:a,c;
(4)N点所示的c溶液为某温度下c的不饱和溶液.C的不饱和溶液转化为饱和溶液的方法有蒸发水分、增加溶质、升高温度,转化为饱和溶液后浓度不一定增大,故填:不饱和,蒸发水分、增加溶质、升高温度,错;
(5)将t1℃时,a、b、c三种物质饱和溶液的温度升高到t2℃时,ab的溶解度都增大,但是溶液组成不变,故溶质质量分数不变,c的溶解度减小,会析出固体,故溶质质量分数会减小,故其大小关系为b>a>c,观察选项,故填:D;
(6)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,镁与盐酸反应会放出热量,温度升高,同时烧杯中出现浑浊,说明烧杯中的物质的溶解度随温度的升高而减小,故是c物质,故填:c.
(2)P点时a和c的溶解度相交,表示在t1℃时ac的溶解度相等;该温度下a物质的溶解度是20g,若将a物质溶液恒温蒸发20g水,会有a晶体
| 20g |
| 100g |
| 20g |
| 120g |
| 1 |
| 2 |
(3)t2℃时,a的溶解度受温度影响变化大,等质量的a、b、c的饱和溶液,冷却到t1℃,析出晶体最多的是a,c的溶解度随温度的降低而正大,没有晶体析出,故填:a,c;
(4)N点所示的c溶液为某温度下c的不饱和溶液.C的不饱和溶液转化为饱和溶液的方法有蒸发水分、增加溶质、升高温度,转化为饱和溶液后浓度不一定增大,故填:不饱和,蒸发水分、增加溶质、升高温度,错;
(5)将t1℃时,a、b、c三种物质饱和溶液的温度升高到t2℃时,ab的溶解度都增大,但是溶液组成不变,故溶质质量分数不变,c的溶解度减小,会析出固体,故溶质质量分数会减小,故其大小关系为b>a>c,观察选项,故填:D;
(6)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,镁与盐酸反应会放出热量,温度升高,同时烧杯中出现浑浊,说明烧杯中的物质的溶解度随温度的升高而减小,故是c物质,故填:c.
点评:本题难度不大,主要考查了固体溶解度曲线的意义及根据固体的溶解度曲线解决相关的问题.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
 已知反应:2A+3B2=2AB3,该反应中两种反应物的质量关系如图所示,现将16gA和15gB2混合,在一定条件下,充分反应后生成AB3的质量为( )
已知反应:2A+3B2=2AB3,该反应中两种反应物的质量关系如图所示,现将16gA和15gB2混合,在一定条件下,充分反应后生成AB3的质量为( )| A、31g | B、25g |
| C、24g | D、18g |
化学基本概念是化学基础知识的重要组成部分,下列各组的两个概念中,后者包括前者的是( )
| A、中和反应 复分解反应 |
| B、无机物 有机物 |
| C、单质 化合物 |
| D、化合物 氧化物 |
下列关于相对原子质量的说法,正确的是( )
| A、相对原子质量只是一个比值,它的单位为1 |
| B、相对原子质量是由原子的最外层电子数决定的 |
| C、相对原子质量是一个原子的质量,以克为单位 |
| D、相对原子质量是一个原子的质量,以千克为单位 |
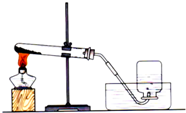 结合“加热高锰酸钾制取氧气”的实验,回答下列问题:
结合“加热高锰酸钾制取氧气”的实验,回答下列问题: 化学课上,同学们做了人体呼出的气体使澄清石灰水变浑浊的实验后,对呼出的气体中主要成分及含量非常好奇,设计实验进行探究.
化学课上,同学们做了人体呼出的气体使澄清石灰水变浑浊的实验后,对呼出的气体中主要成分及含量非常好奇,设计实验进行探究.