题目内容
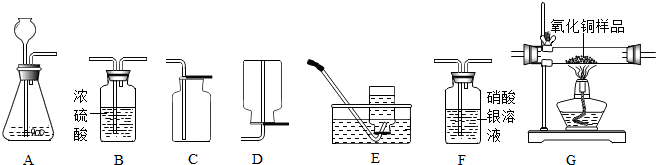
如图为实验室中常见的气体制备、干燥和性质实验的部分仪器.

请回答下列问题:
(1)若实验室用大理石和稀盐酸反应制取并收集一瓶干燥的二氧化碳,
①所选仪器的连接顺序为________(填写仪器序号字母).
②生成二氧化碳的化学方程式为:________.
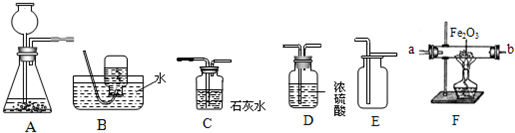
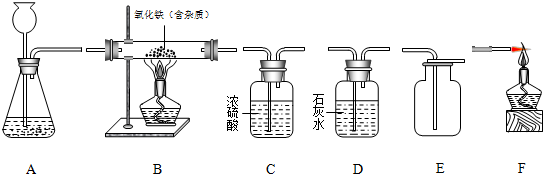
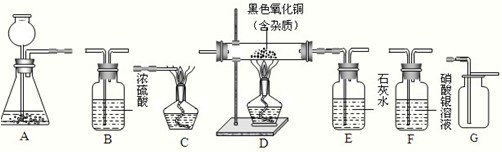
(2)现有一混合气体,其主要成分为CO,含有少量水蒸气,还可能含有少量HCl气体.某化学课题组的同学欲用该混合气体进行实验:
①检验HCl气体是否存在,并除去HCl气体;
②用干燥纯净的CO气体还原不纯的氧化铜试样(其中的杂质不发生变化);
③实验CO气体还原氧化铜生成的气体生成物的性质.
试用如图所示的仪器组装一套实验装置,完成上述实验任务.
①实验进行时,若要气体从左向右流动,则这几种仪器组件的连接顺序应是(填写仪器装置):________.
②判定HCl气体是否存在的根据是________.
③若反应进行完全后,若仪器E中物质增重a g,则仪器D中的试样质量减少________g.
④若原混合气体中混有二氧化碳,反应进行完全后,若通过仪器E中物质增重来计算样品中氧化铜的纯度,测算结果将________(填“偏小”“偏大”“不受影响”之一).
解:(1)在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;这时二氧化碳中混有氯化氢气体和水蒸气,氯化氢气体用硝酸银溶液检验并吸收;浓硫酸可以干燥二氧化碳.故答案为:A、F、B、G;CaCO3+2HCl=CaCl2+H2O+CO2↑
(2)一氧化碳中混有杂质氯化氢气体和水蒸气,氯化氢气体用硝酸银溶液检验并吸收,如果有白色沉淀生成,就一定有氯化氢气体;浓硫酸可以干燥二氧化碳和一氧化碳.若反应进行完全后,若仪器E中物质增重a g,设氧化铜的质量是x
CO+CuO Cu+CO2
Cu+CO2
80 44
x ag x=
x= g 减少的质量是氧元素的质量,质量为:
g 减少的质量是氧元素的质量,质量为: ×
× ≈0.36g
≈0.36g
若原混合气体中混有二氧化碳,反应进行完全后,若通过仪器E中物质增重来计算样品中氧化铜的纯度,测算结果将偏大.故答案为:F、B、D、E、C;F中是否有白色沉淀生成;0.36a;偏大.
分析:实验室用大理石和稀盐酸反应制取并收集一瓶干燥的二氧化碳,在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;这时二氧化碳中混有氯化氢气体和水蒸气,氯化氢气体用硝酸银溶液检验并吸收,如果有白色沉淀生成,就一定有氯化氢气体;浓硫酸可以干燥二氧化碳和一氧化碳.一氧化碳还原氧化铜生成铜和二氧化碳,二氧化碳能使澄清的石灰水变浑浊;根据化学方程式的计算可以求D中减少的质量;若原混合气体中混有二氧化碳,反应进行完全后,若通过仪器E中物质增重来计算样品中氧化铜的纯度,测算结果将偏大.
点评:本题考查的是气体的干燥、除杂和化学方程式的书写等,综合性比较强.要知道浓硫酸是常用的干燥剂,氯化氢气体一般用硝酸银溶液检验并吸收,二氧化碳一般用石灰水检验,有关的计算要准确.本考点是中考的重要考点之一,主要出现在选择题和实验题中.
(2)一氧化碳中混有杂质氯化氢气体和水蒸气,氯化氢气体用硝酸银溶液检验并吸收,如果有白色沉淀生成,就一定有氯化氢气体;浓硫酸可以干燥二氧化碳和一氧化碳.若反应进行完全后,若仪器E中物质增重a g,设氧化铜的质量是x
CO+CuO
 Cu+CO2
Cu+CO2 80 44
x ag
 x=
x= g 减少的质量是氧元素的质量,质量为:
g 减少的质量是氧元素的质量,质量为: ×
× ≈0.36g
≈0.36g若原混合气体中混有二氧化碳,反应进行完全后,若通过仪器E中物质增重来计算样品中氧化铜的纯度,测算结果将偏大.故答案为:F、B、D、E、C;F中是否有白色沉淀生成;0.36a;偏大.
分析:实验室用大理石和稀盐酸反应制取并收集一瓶干燥的二氧化碳,在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;这时二氧化碳中混有氯化氢气体和水蒸气,氯化氢气体用硝酸银溶液检验并吸收,如果有白色沉淀生成,就一定有氯化氢气体;浓硫酸可以干燥二氧化碳和一氧化碳.一氧化碳还原氧化铜生成铜和二氧化碳,二氧化碳能使澄清的石灰水变浑浊;根据化学方程式的计算可以求D中减少的质量;若原混合气体中混有二氧化碳,反应进行完全后,若通过仪器E中物质增重来计算样品中氧化铜的纯度,测算结果将偏大.
点评:本题考查的是气体的干燥、除杂和化学方程式的书写等,综合性比较强.要知道浓硫酸是常用的干燥剂,氯化氢气体一般用硝酸银溶液检验并吸收,二氧化碳一般用石灰水检验,有关的计算要准确.本考点是中考的重要考点之一,主要出现在选择题和实验题中.

练习册系列答案
 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目