题目内容
如图所示为实验室中常见的气体制备、净化、收集和性质实验的部分仪器.据题目要求,回答下列问题:
(1)欲在实验室中制备并收集干燥的二氧化碳.
①所选仪器的连接顺序为 (填写仪器序号字母).
②仪器A中,发生反应的化学方程式为 .
(2)在实验室制取CO2气体后剩余溶液中一定有CaCl2,可能有HCl(杂质不溶于水且不参加反应).为验证是否含有HCl,可在剩余溶液样品中直接加入一种物质,在提供的铁粉、AgNO3溶液、紫色石蕊试液三种试剂中,选择一种试剂进行试验,简述理由 .
(3)欲用足量纯净的一氧化碳气体测定某10g不纯氧化铁样品的纯度(杂质不反应),并验证反应中气体生成物的性质.所选仪器的连接顺序为:纯净的一氧化碳气体→D→B→C.
①仪器C的作用是 .
②反应完全后,计算氧化铁样品的纯度时,小强同学认为“仪器D中减少的质量等于仪器B中增加的质量”,你认为小强的观点 (填“正确”或“不正确”).经测定仪器B反应后比反应前增重了6.6g,则此氧化铁样品的纯度为 .

(1)欲在实验室中制备并收集干燥的二氧化碳.
①所选仪器的连接顺序为
②仪器A中,发生反应的化学方程式为
(2)在实验室制取CO2气体后剩余溶液中一定有CaCl2,可能有HCl(杂质不溶于水且不参加反应).为验证是否含有HCl,可在剩余溶液样品中直接加入一种物质,在提供的铁粉、AgNO3溶液、紫色石蕊试液三种试剂中,选择一种试剂进行试验,简述理由
(3)欲用足量纯净的一氧化碳气体测定某10g不纯氧化铁样品的纯度(杂质不反应),并验证反应中气体生成物的性质.所选仪器的连接顺序为:纯净的一氧化碳气体→D→B→C.
①仪器C的作用是
②反应完全后,计算氧化铁样品的纯度时,小强同学认为“仪器D中减少的质量等于仪器B中增加的质量”,你认为小强的观点
考点:二氧化碳的实验室制法,气体的干燥(除水),一氧化碳的化学性质,酸的化学性质,根据化学反应方程式的计算
专题:碳单质与含碳化合物的性质与用途,常见气体的实验室制法、检验、干燥与净化
分析:(1)①根据反应物的状态和反应条件确定实验室制取气体的发生装置,根据气体的密度和溶水性确定气体的收集装置,要得到干燥的二氧化碳,应在收集装置前面加一个干燥装置;
②根据化学方程式的写法写出实验室制取二氧化碳的反应原理;
(2)根据盐酸的化学性质来分析;
(3)①一氧化碳气和氧化铁不能完全反应,所以尾气中还有一氧化碳;
②根据化学方程式进行分析判断,并根据二氧化碳的质量计算氧化铁的质量,进而求质量分数.
②根据化学方程式的写法写出实验室制取二氧化碳的反应原理;
(2)根据盐酸的化学性质来分析;
(3)①一氧化碳气和氧化铁不能完全反应,所以尾气中还有一氧化碳;
②根据化学方程式进行分析判断,并根据二氧化碳的质量计算氧化铁的质量,进而求质量分数.
解答:解:(1)①实验室通常用稀盐酸与大理石反应制取二氧化碳,反应物的状态是固态和液态,反应条件是常温,应选固-液不加热型的发生装置;二氧化碳的密度比空气大,能溶于水,不能用排水法收集;因为要收集到干燥的二氧化碳,所以应在收集装置前面加一个干燥装置,浓硫酸具有吸水性,可用来干燥二氧化碳,所以仪器的连接顺序为:A→E→F;
②实验室制取二氧化碳的反应物是碳酸钙和盐酸,生成物是氯化钙、水、二氧化碳,有关化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)为验证是否含有HCl,一定不能加入的是的是AgNO3,理由是CaCl2、HCl都能与AgNO3溶液反应生成沉淀;可以用铁粉或紫色石蕊试液来验证;因此可以取少量铁粉于试管中,向其中滴加剩余溶液,若有气体生成则剩余溶液中含有HCl,若不产生气体,则溶液中无HCl;
(3)①一氧化碳气和氧化铁不能完全反应,所以尾气中还有一氧化碳,如不除去会污染空气,因此仪器C的作用是尾气处理,防止污染环境;
②反应的化学方程式为:3CO+Fe2O3
2Fe+3CO2,由此可知,仪器D中减少的质量为氧花铁中氧元素的质量,仪器B中增加的质量为二氧化碳的质量,小强的观点不正确;
设氧化铁样品中氧化铁的质量为x
3CO+Fe2O3
2Fe+3CO2
160 132
x 6.6g
=
解得:x=8g
氧化铁样品的纯度为:
×100%=80%.
故答案为:(1)①AEF;
②CaCO3+2HClCaCl2+H2O+CO2↑;
(2)取少量铁粉于试管中,向其中滴加剩余溶液,若有气体生成则剩余溶液中含有HCl,若不产生气体,则溶液中无HCl;
(3)①尾气处理,防止污染环境;
②不正确; 80%
②实验室制取二氧化碳的反应物是碳酸钙和盐酸,生成物是氯化钙、水、二氧化碳,有关化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)为验证是否含有HCl,一定不能加入的是的是AgNO3,理由是CaCl2、HCl都能与AgNO3溶液反应生成沉淀;可以用铁粉或紫色石蕊试液来验证;因此可以取少量铁粉于试管中,向其中滴加剩余溶液,若有气体生成则剩余溶液中含有HCl,若不产生气体,则溶液中无HCl;
(3)①一氧化碳气和氧化铁不能完全反应,所以尾气中还有一氧化碳,如不除去会污染空气,因此仪器C的作用是尾气处理,防止污染环境;
②反应的化学方程式为:3CO+Fe2O3
| ||
设氧化铁样品中氧化铁的质量为x
3CO+Fe2O3
| ||
160 132
x 6.6g
| 160 |
| 132 |
| x |
| 6.6g |
解得:x=8g
氧化铁样品的纯度为:
| 8g |
| 10g |
故答案为:(1)①AEF;
②CaCO3+2HClCaCl2+H2O+CO2↑;
(2)取少量铁粉于试管中,向其中滴加剩余溶液,若有气体生成则剩余溶液中含有HCl,若不产生气体,则溶液中无HCl;
(3)①尾气处理,防止污染环境;
②不正确; 80%
点评:本题涉及知识点较多,难度较大,做题时要认真分析.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
为了防止小包装食品受潮,在一些仪器包装袋中放入的干燥剂是( )
| A、浓硫酸 | B、氢氧化钠 |
| C、熟石灰 | D、生石灰 |
下列实验操作正确的是( )
A、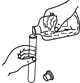 倾倒液体 |
B、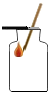 氧气验满 |
C、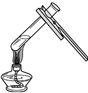 液体加热 |
D、 量9.5mL液体 |
下列有关物质的用途叙述不正确的是( )
| A、食盐可作调味品及防腐剂 |
| B、纯碱可消除面团发酵时产生的酸性 |
| C、硝酸铵(NH4NO3)可作复合肥料 |
| D、硫酸铜可用来配制波尔多农药 |
 如图所示,向小试管中分别加入下列一定量的物质,U型管中的液面将出现左侧高于右侧液面的变化,该物质是( )
如图所示,向小试管中分别加入下列一定量的物质,U型管中的液面将出现左侧高于右侧液面的变化,该物质是( )| A、浓硫酸 | B、氢氧化钠固体 |
| C、蔗糖固体 | D、硝酸铵固体 |
区别H2、O2、CO2三种气体能够成功的方法是( )
| A、将气体分别通人灼热的CuO |
| B、将气体分别用燃着的木条试验 |
| C、将气体分别通人澄清的石灰水里 |
| D、将气体分别通过灼热的铜丝 |
