题目内容
 测定空气中氧气含量的实验如图所示.
测定空气中氧气含量的实验如图所示.实验步骤如下:
①在集气瓶内加入少量水,并做好标记,将标记以上的部分按体积分成5等份;
②检查装置的气密性;
③在燃烧匙内装入足量红磷,将导管上的止水夹夹紧,在酒精灯上点燃红磷,立即伸入集气瓶中塞紧橡皮塞;
④充分反应后,待集气瓶冷却到室温,打开止水夹.
请你根据实验完成下列问题:
(1)步骤③中发生反应的符号表达式:
(2)该实验中红磷稍过量,目的是
(3)待红磷熄灭并冷却后,打开弹簧夹,观察到烧杯中的水进入集气瓶,瓶内水面最终上升约至1刻度处.由此可知氧气约占空气总体积的
(4)红磷熄灭后,集气瓶内剩下的气体主要是
(5)实验完毕,发现进入集气瓶中的水的体积不到容积的
| 1 |
| 5 |
考点:空气组成的测定,书写化学方程式、文字表达式、电离方程式
专题:空气与水
分析:(1)根据红磷燃烧的反应、现象分析回答;
(2)根据实验的目的分析红磷稍过量的原因;
(3)根据实验的现象分析空气中氧气的含量;
(4)根据集气瓶内剩余的气体主要是氮气和实验的现象分析氮气的性质;
(5)根据实验的注意的事项分析实验不成功的原因.
(2)根据实验的目的分析红磷稍过量的原因;
(3)根据实验的现象分析空气中氧气的含量;
(4)根据集气瓶内剩余的气体主要是氮气和实验的现象分析氮气的性质;
(5)根据实验的注意的事项分析实验不成功的原因.
解答:解:(1)步骤③中红磷燃烧生成了五氧化二磷,发生反应的符号表达式:4P+5O2
2P2O5;观察到的现象是:红磷燃烧,产生大量的白烟;
(2)该实验是测定空气中氧气的含量,必需将氧气全部消耗掉,所以红磷稍过量,目的是:全部消耗掉集气瓶内空气中的氧气;
(3)待红磷燃烧消耗了氧气,熄灭并冷却后,打开弹簧夹,观察到烧杯中的水进入集气瓶,瓶内水面最终上升约至1刻度处.由此可知:氧气约占空气总体积的
.
(4)红磷熄灭后,集气瓶内剩下的气体主要是氮气,由水倒流入集气瓶中的体积只有
,说明了氮气难溶于水;由红磷燃烧一会熄灭了,说明氮气不燃烧不支持燃烧,其化学性质不活泼.
(5)实验完毕,发现进入集气瓶中的水的体积不到容积的
,导致这一结果的原因可能是:红磷的量不足; 装置漏气;未冷却至室温就打开了弹簧夹.
故答为:(1)4P+5O2
2P2O5,红磷燃烧,产生大量的白烟;
(2)全部消耗掉集气瓶内空气中的氧气;(3)
;(4)难,不活泼;(5)红磷的量不足; 装置漏气.
| ||
(2)该实验是测定空气中氧气的含量,必需将氧气全部消耗掉,所以红磷稍过量,目的是:全部消耗掉集气瓶内空气中的氧气;
(3)待红磷燃烧消耗了氧气,熄灭并冷却后,打开弹簧夹,观察到烧杯中的水进入集气瓶,瓶内水面最终上升约至1刻度处.由此可知:氧气约占空气总体积的
| 1 |
| 5 |
(4)红磷熄灭后,集气瓶内剩下的气体主要是氮气,由水倒流入集气瓶中的体积只有
| 1 |
| 5 |
(5)实验完毕,发现进入集气瓶中的水的体积不到容积的
| 1 |
| 5 |
故答为:(1)4P+5O2
| ||
(2)全部消耗掉集气瓶内空气中的氧气;(3)
| 1 |
| 5 |
点评:本题考查学生对实验原理与实验操作的理解与评价等,难度中等,清楚实验原理是解题的关键,需要学生具备扎实的基础知识与综合运用知识分析问题、解决问题的能力.

练习册系列答案
相关题目
图表资料可以为我们提供很多信息,下列是某学生对图表资料的使用,其中正确的是( )
| A、根据元素周期表查某元素的原子序数或质子数 |
| B、根据原子的结构示意图可确定该原子的核内中子数 |
| C、根据酸碱盐的溶解性表,判断复分解反应能否进行 |
| D、根据相对原子质量表,判断某种元素原子的核外电子数目 |
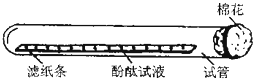 将滴有酚酞试液的滤纸条放在试管里,如图所示放在实验台上.
将滴有酚酞试液的滤纸条放在试管里,如图所示放在实验台上.
 如图是某同学用高锰酸钾制氧气的实验装置图
如图是某同学用高锰酸钾制氧气的实验装置图
 某校化学兴趣小组的同学取60g氯化钙溶液,向其中加入适量碳酸钠溶液,反应完毕后过滤,所得固体用作制取牙膏摩擦剂的主要原料,同时所得滤液用来进行小麦选种(选种液要求氯化钠是质量分数在10%~20%之间).实验过程中所加碳酸钠溶液的质量与生成碳酸钙沉淀的质量关系如下图所示.通过下图可知,当氯化钙恰好反应完时:
某校化学兴趣小组的同学取60g氯化钙溶液,向其中加入适量碳酸钠溶液,反应完毕后过滤,所得固体用作制取牙膏摩擦剂的主要原料,同时所得滤液用来进行小麦选种(选种液要求氯化钠是质量分数在10%~20%之间).实验过程中所加碳酸钠溶液的质量与生成碳酸钙沉淀的质量关系如下图所示.通过下图可知,当氯化钙恰好反应完时: 请回答下列问题:
请回答下列问题: