题目内容
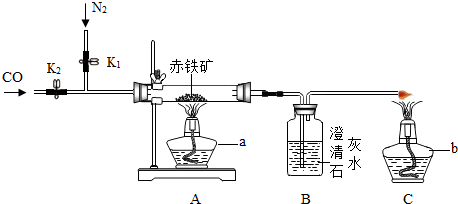
用CO还原赤铁矿(主要成分是Fe2O3)样品12g,将反应生成的CO2气体,全部通过入过量的石灰水中,生成白色沉淀15g,试计算原赤铁矿中氧化铁的质量分数.分析:本题涉及两个化学反应方程式:Fe2O3+3CO
2Fe+3CO2 和 CO2+Ca(OH)2═CaCO3↓+H2O,二者之间可通过二氧化碳相联系,根据后一个方程式15g白色沉淀,即生成15g碳酸钙的质量可以求出二氧化碳的质量,再根据二氧化碳的质量,利用前一个方程式可求出氧化铁的质量,进一步可求出样品中Fe2O3的质量分数.
| ||
解答:解:设生成3.0g碳酸钙需要二氧化碳的质量为x
CO2+Ca(OH)2═CaCO3↓+H2O
44 100
x 15g
=
x=6.6g
设生成6.6g二氧化碳需要Fe2O3的质量为y
Fe2O3+3CO
2Fe+3CO2
160 132
y 6.6g
=
y=8g
赤铁矿样品中Fe2O3的质量分数为:
×100%=66.67%
答:赤铁矿样品中Fe2O3的质量分数为66.67%
CO2+Ca(OH)2═CaCO3↓+H2O
44 100
x 15g
| 44 |
| 100 |
| x |
| 15g |
x=6.6g
设生成6.6g二氧化碳需要Fe2O3的质量为y
Fe2O3+3CO
| ||
160 132
y 6.6g
| 160 |
| y |
| 132 |
| 6.6g |
y=8g
赤铁矿样品中Fe2O3的质量分数为:
| 8g |
| 12g |
答:赤铁矿样品中Fe2O3的质量分数为66.67%
点评:本题考查有关化学反应方程式的计算,在计算时一定要找准相关量之间的对应关系.

练习册系列答案
相关题目