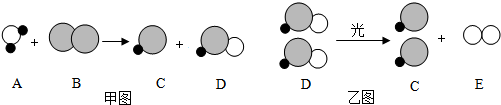
题目内容
现有32g某可燃物质在密闭容器中完全燃烧后,测得生成88g二氧化碳气体和72g水蒸气,则下列说法正确的是( )
| A、该可燃物一定含有碳、氢元素,可能含有氧元素 |
| B、该可燃物只含有碳、氢两种元素 |
| C、该可燃物的化学式中碳元素与氢元素的原子个数比为3:1 |
| D、该可燃物中氢元素的质量分数为25% |
考点:质量守恒定律及其应用,元素的质量分数计算
专题:化学用语和质量守恒定律
分析:化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和.
解答:解:参加反应的氧气质量为:88g+72g-32g=128g,
88g二氧化碳中碳元素的质量为:88g×
×100%=24g,氧元素的质量为:88g-24g=64g,
72g水中氢元素的质量为:72g×
×100%=8g,氧元素的质量为:72g-8g=64g,
二氧化碳中的碳元素和水中的氢元素来自于该可燃物,该可燃物中氧元素的质量为:64g+64g-128g=0,
则该可燃物只含有碳、氢两种元素;
该可燃物的化学式中碳元素与氢元素的原子个数比为:
:
=1:4;
该可燃物中氢元素的质量分数为:
×100%═25%
故选:BD.
88g二氧化碳中碳元素的质量为:88g×
| 12 |
| 44 |
72g水中氢元素的质量为:72g×
| 2 |
| 18 |
二氧化碳中的碳元素和水中的氢元素来自于该可燃物,该可燃物中氧元素的质量为:64g+64g-128g=0,
则该可燃物只含有碳、氢两种元素;
该可燃物的化学式中碳元素与氢元素的原子个数比为:
| 24g |
| 12 |
| 8g |
| 1 |
该可燃物中氢元素的质量分数为:
| 8g |
| 32g |
故选:BD.
点评:化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、进行相关方面计算的基础.

练习册系列答案
相关题目
合成气【CO、H2】在不同催化剂作用下,可以合成不同的物质.仅用合成气为原料可能得到的物质是( )
| A、酒精(C2H6O) |
| B、尿素[CO(NH2)2] |
| C、甲醇(CH3OH) |
下列关于化学反应2X+Y═2Z的叙述,错误的是( )
| A、Z一定是化合物 |
| B、在反应中X、Y、Z三种物质的粒子数目比为2:1:2 |
| C、若X和Y的相对分子质量分别为m和n,则Z的相对分子质量为(m+n) |
| D、若a g X完全反应生成b g Z,则同时消耗(b-a)g Y |
化学用语是学习和交流化学知识的通用语言.以下化学符号表示意义最多的是( )
| A、2H2O |
| B、N |
| C、N2 |
| D、Fe |
一杯氯化钠溶液,测的上层密度是A,下层密度是B则A与B的关系是( )
| A、A>B | B、A<B |
| C、A=B | D、无法确定 |
 氯原子,
氯原子, 氧原子,
氧原子, 氢原子)( D的化学式为HClO)
氢原子)( D的化学式为HClO)