题目内容
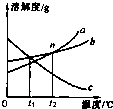 如图为a、b、c三种物质的溶解度曲线.
如图为a、b、c三种物质的溶解度曲线.(1)要增大c物质的溶解度,可采取的方法是
降低温度
降低温度
.(2)t2℃时,将a、b、c饱和溶液降温到t1℃,溶液中溶质质量分数大小为
b>a>c
b>a>c
.(3)要将a、b、c三种物质的不饱和溶液变成饱和,均可采用的方法是
增加溶质或蒸发溶剂
增加溶质或蒸发溶剂
.分析:(1)由c物质的溶解度曲线,c物质的溶解度随温度的升高而减小,据此判断增大c物质的溶解度可采取的方法.
(2)根据t2℃时、t1℃时三种物质的溶解度大小,判断降温后是否会析出晶体,结合饱和溶液中溶质质量分数=
×100%,进行分析解答.
(3)根据溶解度曲线图象可知,a、b物质的溶解度随温度的升高而增大,c物质的溶解度随温度的升高而减小,故要将a、b、c三种物质的不饱和溶液变成饱和不能同时采用相同的改变温度的方法,据此进行分析解答.
(2)根据t2℃时、t1℃时三种物质的溶解度大小,判断降温后是否会析出晶体,结合饱和溶液中溶质质量分数=
| 溶解度 |
| 溶解度+100g |
(3)根据溶解度曲线图象可知,a、b物质的溶解度随温度的升高而增大,c物质的溶解度随温度的升高而减小,故要将a、b、c三种物质的不饱和溶液变成饱和不能同时采用相同的改变温度的方法,据此进行分析解答.
解答:解:(1)根据溶解度曲线图象可知,c物质的溶解度随温度的升高而减小,故要增大c物质的溶解度,可采取降低温度的方法.
(2)由于在t2℃时,三种物质的溶解度大小关系是a=b>C,即在t2℃时,三种物质的饱和溶液中溶质的质量分数:a=b>C;由于a和b的溶解度随温度的降低而减小,因此降温至t1℃时,a和b的溶液中都会有晶体析出,溶液都还是饱和溶液,由于在t1℃时三种物质的溶解度b=c>a,而由于c的溶解度随温度的降低而增大,因此降温至t1℃时,它的饱和溶液就会变成不饱和溶液,但溶液中溶质的质量分数不变;由图可知,t1℃时a的溶解度大于t2℃时c的溶解度,c的溶液中溶质的质量分数还是最小,故溶液中溶质质量分数大小为b>a>c.
(3)根据溶解度曲线图象可知,a、b物质的溶解度随温度的升高而增大,c物质的溶解度随温度的升高而减小,故要将a、b、c三种物质的不饱和溶液变成饱和不能同时采用相同的改变温度的方法,均可采用增加溶质或蒸发溶剂的方法.
故答案为:(1)降低温度;(2)b>a>c;(3)增加溶质或蒸发溶剂.
(2)由于在t2℃时,三种物质的溶解度大小关系是a=b>C,即在t2℃时,三种物质的饱和溶液中溶质的质量分数:a=b>C;由于a和b的溶解度随温度的降低而减小,因此降温至t1℃时,a和b的溶液中都会有晶体析出,溶液都还是饱和溶液,由于在t1℃时三种物质的溶解度b=c>a,而由于c的溶解度随温度的降低而增大,因此降温至t1℃时,它的饱和溶液就会变成不饱和溶液,但溶液中溶质的质量分数不变;由图可知,t1℃时a的溶解度大于t2℃时c的溶解度,c的溶液中溶质的质量分数还是最小,故溶液中溶质质量分数大小为b>a>c.
(3)根据溶解度曲线图象可知,a、b物质的溶解度随温度的升高而增大,c物质的溶解度随温度的升高而减小,故要将a、b、c三种物质的不饱和溶液变成饱和不能同时采用相同的改变温度的方法,均可采用增加溶质或蒸发溶剂的方法.
故答案为:(1)降低温度;(2)b>a>c;(3)增加溶质或蒸发溶剂.
点评:本题难度不大,主要考查了固体溶解度曲线所表示的意义,通过本题可以加强学生对固体溶解度的理解,培养学生应用知识解决问题的能力

练习册系列答案
相关题目
 13、(1)用化学用语表示:
13、(1)用化学用语表示: 18、如图为a、b、c三种物质的溶解度曲线,根据曲线回答下列问题.
18、如图为a、b、c三种物质的溶解度曲线,根据曲线回答下列问题. 23、如图为A、B、C三种物质的溶解度曲线.据此回答:
23、如图为A、B、C三种物质的溶解度曲线.据此回答: 如图为A、B、C三种物质的溶解度曲线,据图回答:
如图为A、B、C三种物质的溶解度曲线,据图回答: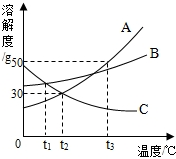 如图为A、B、C三种固体物质的溶解度曲线,请回答:
如图为A、B、C三种固体物质的溶解度曲线,请回答: