题目内容
【题目】结合图1化学实验装置,回答有关问题。
I某化学兴趣小组进行如下系列实验。请根据下图回答问题:
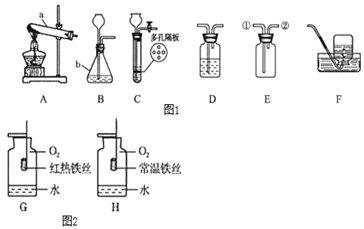
(1)写出图中标有宇母的仪器的名称: b__________
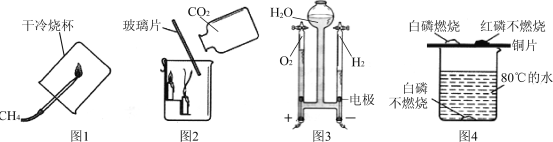
(2)写出实验室用A装置取氧气的化学方程式 ______ ,制得的氧气用来做如图2所示的实验,发现H中铁丝不燃烧,其原因是_________。
(3)实验室制取二氧化碳常用的药品是_____,若用装置E收集二氧化碳,则气体应从_____ 填 “①”或“②“)端进入;若要获得干燥的二氧化碳,可将装置B和装置D用胶皮管连接,并在装置D中盛放___________(填物质名称)试剂。
(4)实验室常用装置C代替装置B制取气体,装置C的优点是__________
II某化学兴趣小组的同学,通过咨询老师准备用亚硫酸钠溶液与浓硫酸反应来制备一定量的SO2(Na2SO3+H2SO4(浓)==Na2SO4+SO2↑+H2O]。老师给他们提供了一瓶亚硫酸钠溶液并告知该瓶溶液放置时间可能较长,不知是否变质。兴趣小组的同学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
(提出问题)①该瓶溶液中溶质的成分是什么?②该瓶溶液中亚硫酸钠的质量分数是多少?
(查阅资料)
(1)Na2SO3有较强还原性,在空气中易被氧气氧化:2 Na2SO3+O2==2Na2SO4;
(2)Na2SO3能与酸反应产生SO2气体;
(3)SO32-、SO42-均能与Ba2+反应产生白色沉淀,BaSO3可溶于稀盐酸。
(作出猜想)
猜想1:没有变质,成分是Na2SO3;猜想2完全变质,成分是Na2SO4;
你认为还可能有的猜想3:_____________________。
(实验探究I)甲、乙两组分别进行实验探究溶液是否变质:
小组 | 实验操作 | 现象 | 结论 |
甲组 | 取少量样品于试管中加入过量稀盐酸 | 产生气泡 | 没有变质,还是Na2SO3 |
乙组 | 取少量样品于试管中加入氯化钡溶液,再加入足量稀盐酸 | _____ | 已部分变质 |
(评价)有同学质疑甲组方案不合理,理由是___________。
(实验探究II)
甲组设计如下实验测定Na2SO3溶液的溶质质量分数。(注:空气中二氧化碳的影响忽略不计)
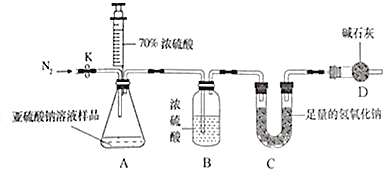
(1)连好装置并检查装置气密性,在锥形瓶中放入126g该样品
(2)实验前称量C装置的质量;
(3)关闭活塞K,用注射器推入浓硫酸至不再产生气泡;
(4)打开活塞K,缓缓鼓入一定量的氮气,关闭活塞K;
(5)再次称量C装置的质量发现比反应前增重6.4g。
D装置的作用为_____________ , 计算出该溶液中Na2SO3的质量分数为______;
(解释)若没有进行第4步操作,则测得亚硫酸钠溶液的溶质质量分数比实际的____(填”偏小”或”偏大”)。(反思)由此可得出,保存亚硫酸钠时应__________。
【答案】锥形瓶 2KC1O3![]() 2KC1+3O2↑ 温度没有达到着火点 石灰石和稀盐酸 ① 浓硫酸 控制反应进行 部分变质成分是Na2SO3和 Na2SO4的混合物 产生白色沉淀,加入稀盐酸后有气泡产生,沉淀部分消失 部分变质也有气泡产生 防止空气中的水和二氧化碳进入C装置 10% 偏小 密封保存,防止氧化
2KC1+3O2↑ 温度没有达到着火点 石灰石和稀盐酸 ① 浓硫酸 控制反应进行 部分变质成分是Na2SO3和 Na2SO4的混合物 产生白色沉淀,加入稀盐酸后有气泡产生,沉淀部分消失 部分变质也有气泡产生 防止空气中的水和二氧化碳进入C装置 10% 偏小 密封保存,防止氧化
【解析】
I、(1)据图可知仪器b是锥形瓶;
(2)装置A适用于固体加热制取气体,因为试管口没有棉花团,所以是加热氯酸钾与二氧化锰的混合物制取氧气,同时生成氯化钾,化学方程式:2KC1O3![]() 2KC1+3O2↑;制得的氧气用来做如图2所示的实验,发现H中铁丝不燃烧,其原因是温度没有达到铁丝的着火点或氧气不纯;
2KC1+3O2↑;制得的氧气用来做如图2所示的实验,发现H中铁丝不燃烧,其原因是温度没有达到铁丝的着火点或氧气不纯;
(3)在实验室中常用大理石或石灰石与稀盐酸反应来制取二氧化碳,二氧化碳的密度比空气大,若用装置E收集二氧化碳,则气体应从①端进入;浓硫酸具有吸水性,若要获得干燥的二氧化碳,可将装置B和装置D用胶皮管连接,并在装置D中盛放浓硫酸;
(4)实验室常用装置C代替装置B制取气体,装置C的优点是可以控制反应进行与停止;
II、[作出猜想]猜想1:没有变质,成分是Na2SO3;猜想2:完全变质,成分是Na2SO4;猜想3:部分变质,成分是Na2SO3、Na2SO4;
[实验探究Ⅰ]取少量样品于试管中加入过量稀盐酸,产生气泡,说明溶液中含有亚硫酸钠;取少量样品于试管中加入氯化钡溶液,再加入足量稀盐酸,产生白色沉淀,沉淀部分溶解,产生气泡,说明溶液中含有硫酸钠和亚硫酸钠;
[评价]有同学质疑甲组方案不合理,理由是含有硫酸钠和亚硫酸钠的溶液也能和稀盐酸反应生成气体;
[实验探究Ⅱ] D装置的作用为: 防止空气中的水和二氧化碳进入C装置;
再次称量C装置的质量发现比反应前增重6.4g,说明反应生成了6.4g二氧化硫,设亚硫酸钠质量为x,

![]()
x=12.6g,
该溶液中Na2SO3的质量分数为:![]() ×100%=10%;
×100%=10%;
[解释]若没有进行第4步操作,会导致二氧化硫不能被氢氧化钠溶液完全吸收,则测得亚硫酸钠溶液的溶质质量分数比实际的偏小;
[反思]亚硫酸钠容易被空气中的氧气氧化,因此应该密封保存亚硫酸钠。

 通城学典默写能手系列答案
通城学典默写能手系列答案