题目内容
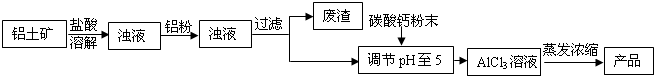
碱式氯化铝是某种高效净水剂的主要成分。实验室利用铝土矿(主要含Al2O3,还含少量Fe2O3及其他不溶杂质)制取碱式氯化铝的过程如下:

(1)溶解过程中,需要使用质量分数为15%的盐酸,则配制这种盐酸需要________mL 30%的浓盐酸(密度约为1.15 g/cm3)和115 g蒸馏水。
(2)盐酸溶解铝土矿过程中,发生反应的化学方程式为:____________________________
(3)加少量铝粉的主要作用是除去浊液中的________。
(4)加CaCO3粉末的作用是调节pH至5。请写出用pH试纸测定溶液pH的操作:在白瓷板或玻璃片上放一小片pH试纸,____________________________________________,得出被测液的pH。
(1)100
(2)Al2O3+6HCl===2AlCl3+3H2O,Fe2O3+6HCl===2FeCl3+3H2O
(3)铁离子(Fe3+)
(4)用玻璃棒蘸取被测液滴到试纸上,把试纸显示的颜色与标准比色卡比较

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目