题目内容
15.我们的家也是一个小小化学实验室呢,细心观察也能学到很多知识.(1)爸爸给家里换了一台节能天然气热水器,天然气的主要成分是CH4,其燃烧的化学方程式为
CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)石墨电极或6B铅笔芯和导线连接在一起,接通电源后灯泡(填“会”或“不会”)发亮,这说明石墨具有导电性.
(3)取一个玻璃杯,放入洗净的碎鸡蛋壳,然后加入一些醋酸,立即用蘸有澄清石灰水的玻璃片盖住,观察到的现象①有气泡产生,②澄清的石灰水变浑浊,由此推测鸡蛋壳中含有碳酸钙.
分析 根据已有的物质的成分以及物质的性质进行分析解答即可.
解答 解:(1)天然气的主要成分是甲烷,燃烧生成二氧化碳和水,故填:CH4,CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(2)铅笔芯的主要成分是石墨,墨电极或6B铅笔芯和导线连接在一起,接通电源后灯泡发光,说明石墨具有导电性,故填:石墨具有导电性;
(3)蛋壳的主要成分是碳酸钙,能与醋酸反应生成二氧化碳气体,会观察到有气泡产生,且澄清的石灰水变浑浊,故填:有气泡产生,澄清的石灰水变浑浊.
点评 本题考查的是常见的物质的用途,完成此题,可以依据已有的物质的性质进行.

练习册系列答案
相关题目
6. 某化学反应的微观示意图如图所示,下列判断不正确的是( )
某化学反应的微观示意图如图所示,下列判断不正确的是( )
 某化学反应的微观示意图如图所示,下列判断不正确的是( )
某化学反应的微观示意图如图所示,下列判断不正确的是( )| A. | 该反应的反应物可能是氨气 | |
| B. | 生成物乙是单质 | |
| C. | 该化学反应中甲、丙、乙的分子个数比为2:1:3 | |
| D. | 根据质量守恒定律可推知,1个乙分子中含有6个A原子 |
20.如图所示的实验操作不正确的是( )
| A. |  铁丝在氧气中燃烧 | B. |  倾倒液体 | ||
| C. |  读取液体的体积 | D. |  制取蒸馏水 |
7.空气中氧气含量测定的再认识
【实验回顾】
图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
(1)写出红磷燃烧的符号表达式4P+5O2 $\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内气压减小,烧杯中水倒吸到集气瓶.若装置气密性良,操作规范.用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量
【提出问题】
有实验资料表明:燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测定结果与理论值往往相差较大.

【实验改进】
Ⅰ.根据铁在空气中生锈的原理设计图2实验装置,再次测定空气中氧气含量.装置中饱和食盐水、活性炭会加速铁生锈
Ⅱ.测得实验数据如表
【交流表达】
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2],写出该反应的化学方程式2Fe+2H2O+O2=2Fe(OH)2
(2)根据表中数据计算,改进实验后测得的空气中氧气的体积分数是20.2%(计算结果精确到0.1%)
(3)从实验原理角度分析,改进后的实验结果比前者准确度更高的原因是①铁的缓慢氧化使集气瓶中的 氧气消耗更彻底,使实验结果更 准确;②测量时考虑到导管容积和扣除内容物后的集气瓶容积,使实验结果更准确.
【实验回顾】
图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
(1)写出红磷燃烧的符号表达式4P+5O2 $\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内气压减小,烧杯中水倒吸到集气瓶.若装置气密性良,操作规范.用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量
【提出问题】
有实验资料表明:燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测定结果与理论值往往相差较大.

【实验改进】
Ⅰ.根据铁在空气中生锈的原理设计图2实验装置,再次测定空气中氧气含量.装置中饱和食盐水、活性炭会加速铁生锈
Ⅱ.测得实验数据如表
| 测量项目 | 实验前 | 实验后 | |
| 烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
| 体积/mL | 80.0 | 54.5 | 126.0 |
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2],写出该反应的化学方程式2Fe+2H2O+O2=2Fe(OH)2
(2)根据表中数据计算,改进实验后测得的空气中氧气的体积分数是20.2%(计算结果精确到0.1%)
(3)从实验原理角度分析,改进后的实验结果比前者准确度更高的原因是①铁的缓慢氧化使集气瓶中的 氧气消耗更彻底,使实验结果更 准确;②测量时考虑到导管容积和扣除内容物后的集气瓶容积,使实验结果更准确.
12.研究和控制化学反应条件有重要意义.
(1)同学们想探究双氧水的溶质质量分数对反应速率的影响,在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
①取用二氧化锰的仪器是图1中的B(选填编号).
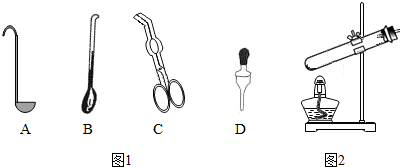
②写出上述反应的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③实验3中,加入的二氧化锰质量为5g.
④相同条件下,实验3产生氧气的速率最快,说明相同条件下,反应物浓度越大,反应速率越快.
(2)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.
(1)同学们想探究双氧水的溶质质量分数对反应速率的影响,在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
| 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 5 | 67 |

②写出上述反应的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③实验3中,加入的二氧化锰质量为5g.
④相同条件下,实验3产生氧气的速率最快,说明相同条件下,反应物浓度越大,反应速率越快.
(2)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.
 如图所示是铁丝在氧气中燃烧的实验,请回答下列问题:
如图所示是铁丝在氧气中燃烧的实验,请回答下列问题: 某兴趣小组的同学设计了如图实验:
某兴趣小组的同学设计了如图实验: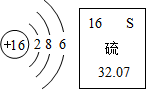 根据图示信息判断,下列说法正确的是C
根据图示信息判断,下列说法正确的是C