题目内容
【题目】请结合下图回答问题:

(1)仪器名称:①______,②______。
(2)用高锰酸钾制取较为纯净的氧气,可选用装置____和 ____组合(选填序号),反应的化学方程式为_______,该实验装置还需要加以改进的地方是_______。
(3)实验室可用装置B或C制H2,C装置相对于B的优点有______。用E装置收集H2,气体应从____(选填“a”或“b”)端通入。
(4)实验室制备二氧化碳,若要检验二氧化碳中是否含有少量氯化氢气体,并得到纯净、干燥的二氧化碳,可将气体依次通过盛有______、______的E装置(选填“AgNO3溶液”、“ 浓NaOH溶液”、“ 紫色石蕊试液”或“浓H2SO4”)。
【答案】铁架台 长颈漏斗 A D 2KMnO4![]() K2MnO4+MnO2+ O2↑ 试管口添加棉花团 控制反应开始和停止(随开随停、节约药品等合理答案给分) a AgNO3溶液 浓H2SO4
K2MnO4+MnO2+ O2↑ 试管口添加棉花团 控制反应开始和停止(随开随停、节约药品等合理答案给分) a AgNO3溶液 浓H2SO4
【解析】
(1)仪器①名称是铁架台,仪器名称;仪器②名称是长颈漏斗;
(2)用高锰酸钾制氧气时,反应物的状态是固体,反应条件是加热,属于固体加热型,发生装置可选用A,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净,收集装置可选用D。用高锰酸钾制取较为纯净的氧气,可选用装置A和D组合;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,反应的化学方程式为:2KMnO4![]() K2MnO4+MnO2+ O2↑;;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;
K2MnO4+MnO2+ O2↑;;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;
(3)用装置C制取氢气时,锌粒放在多孔隔板上,稀硫酸药品从长颈漏斗中加入。反应开始后,关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止,打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行。C装置相对于B的优点有:控制反应开始和停止(随开随停、节约药品等);氢气的密度比空气小,用E装置收集H2,气体应从a(短)管进入;
(4)盐酸与硝酸银反应生成氯化银的沉淀和氯化钠,AgNO3溶液可以检验氯化氢气体并能除去氯化氢气体;浓硫酸具有吸水性,浓H2SO4可以干燥二氧化碳气体,除去水和氯化氢气体时,先除去氯化氢,再除去水。实验室制备二氧化碳,若要检验二氧化碳中是否含有少量氯化氢气体,并得到纯净、干燥的二氧化碳,可将气体依次通过盛有AgNO3溶液、浓H2SO4的E装置。

【题目】某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品(反应的化学方程式:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑),这种工业成为“氯碱工业”,某研究性学习小组对该厂生产的烧碱样品进行如下探究。
2NaOH+H2↑+Cl2↑),这种工业成为“氯碱工业”,某研究性学习小组对该厂生产的烧碱样品进行如下探究。
I.定性探究
(提出问题)烧碱样品中含有哪些杂质?
(猜想)猜想一:可能含有Na2CO3;
猜想二:可能含有NaCl,作出此猜想的依据______(用简洁的文字表述)。
(设计实验)
实验步骤 | 实验现象 | 解释或结论 |
①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁。 | 试管外壁发热 | 原因是 ______ |
②向①所得的溶液中加入稀硝酸至过量,将产生的气体通入澄清石灰水 | 有气体产生,澄清石灰水浑浊 | 样品中含有的杂质是 ______ |
③向②所得的溶液中滴加几滴硝酸银溶液。 | 无现象 | 猜想二 ______ (填“正确”或“错误”) |
(交流与讨论)小明同学提出:“上述实验中稀硝酸也可以用稀盐酸代替”,你同意他的观点吗?若不同意,写出理由______。
Ⅱ.定量探究
(提出问题)烧碱样品中氢氧化钠的质量分数是多少呢?
(设计实验)小丽同学设计探究方案①、②进行实验并测得数据如下:
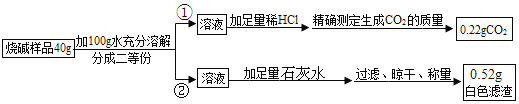
(交流与反思)
(1)小强同学认为方案②因缺少______(填操作名称),导致测得的氢氧化钠的质量分数偏小。
(2)请你利用方案①测得的数据计算烧碱样品中氢氧化钠的质量分数______(请在答题纸上写出计算过程)。


