题目内容
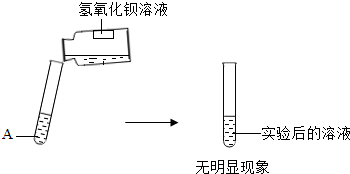
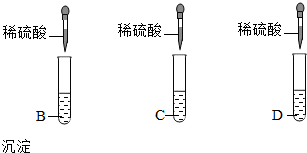
25、有四瓶失去标签的溶液:硝酸钡、碳酸钠、盐酸、稀硫酸,为了鉴别它们做了下列溶液间的某些混合实验,其反应现象如下表.

(1)由表推知(用化学式表示)A
(2)写出相关的反应方程式:

(1)由表推知(用化学式表示)A
HCl
,BNa2CO3
,CBa(NO3)2
,DH2SO4
.(2)写出相关的反应方程式:
2HCl+Na2CO3═2NaCl+H2O+CO2↑,Na2CO3+H2SO4 ═Na2SO4+H2O+CO2↑
.分析:分析所给的四种物质之间能发生反应的为:硝酸钡可以和碳酸钠及稀硫酸反应生成沉淀,碳酸钠能和稀硫酸、盐酸、硝酸钡反应,盐酸可以和碳酸钠反应生成气体,稀硫酸可以和硝酸钡和碳酸钠反应,可以据此来解答该题.
解答:解:(1)从表格中的反应可知:A和B反应生成气体,B和D反应有气体逸出,故可以判断B为碳酸钠,而A和D分别为盐酸和稀硫酸,那么C为硝酸钡,因为硫酸能够和硝酸钡反应生成沉淀,所以根据A和C反应没有现象可以知道A为盐酸,D为稀硫酸,故本题答案为:HCl; Na2CO3; Ba(NO3);2 H2SO4
(2)根据(1)中的解答可以知道A和B的反应为盐酸和碳酸钠的反应,B和D的反应为碳酸钠和硫酸的反应,故本题答案为:
2HCl+Na2CO3═2NaCl+H2O+CO2↑; Na2CO3+H2SO4 ═Na2SO4+H2O+CO2↑
(2)根据(1)中的解答可以知道A和B的反应为盐酸和碳酸钠的反应,B和D的反应为碳酸钠和硫酸的反应,故本题答案为:
2HCl+Na2CO3═2NaCl+H2O+CO2↑; Na2CO3+H2SO4 ═Na2SO4+H2O+CO2↑
点评:熟练掌握酸碱盐的化学性质,并能根据酸碱盐两两之间的反应来判断物质的种类和名称,记住化学方程式:2HCl+Na2CO3═2NaCl+H2O+CO2↑;Na2CO3+H2SO4 ═Na2SO4+H2O+CO2↑

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目