题目内容
19.如图是某个化学反应的微观示意图,从中获取的信息正确的是( )
| A. | 图①分子中两种原子的个数比为1:4 | B. | 反应物和生成物均是化合物 | ||
| C. | 反应前后原子的种类和个数不变 | D. | 该反应是复分解反应 |
分析 观察化学反应的微观示意图,根据物质的微观构成,分析物质的类别;对比反应前后微粒的变化,判断分子、原子的变化;根据反应的特点分析反应的类型.
解答 解:A、由图①分子的微观构成可知,两种原子的个数比为1:2,故A错误;
B、由图物质的微观构成可知,图②对应物质的分子是由同种原子构成的,属于单质,故B不正确;
C、由反应前后物质的微观构成可知,反应前后原子的种类和个数不变,故C正确;
D、由化学反应的微观示意图可知,该反应的反应物是一种化合物和一种单质,不属于复分解反应,故D错误.
故选:C.
点评 解答本题的关键是要充分理解图中提供的信息,充分理解“一种小球代表一种原子”,只有这样才能对问题做出正确的判断.

练习册系列答案
相关题目
9.如图为汽车尾气净化装置中发生反应的微观示意图,有关叙述错误的是( )


| A. | 图中单质的化学式为N2 | B. | 反应前后分子、原子种类均不变 | ||
| C. | 反应后分子总数减少 | D. | 原子是化学变化中的最小微粒 |
10.甲、乙、丙三种物质在水中的溶解度如下表所示(单位:g/100g水),根据数据回答下列问题:
①10℃时,甲的溶解度是64g/100g水;
②20℃时,三种物质的溶解度由大到小依次为甲>丙>乙;
③40℃时,丙的饱和溶液的溶质质量分数为$\frac{37.4}{100+37.4}$×100%(请用相应的数据列式表示,不必计算);
④乙中混有少量的丙,得到较纯净的乙的方法是冷却结晶;
⑤上述数据也可以说明,溶质的性质和温度能够影响物质的溶解性.
| 温度(℃) | 10 | 20 | 40 | 60 | 80 |
| 甲 | 64 | 85 | 138 | 203 | 285 |
| 乙 | 21.2 | 31.6 | 61.3 | 167 | 203 |
| 丙 | 35.8 | 35.9 | 37.4 | 38.0 | 38.5 |
②20℃时,三种物质的溶解度由大到小依次为甲>丙>乙;
③40℃时,丙的饱和溶液的溶质质量分数为$\frac{37.4}{100+37.4}$×100%(请用相应的数据列式表示,不必计算);
④乙中混有少量的丙,得到较纯净的乙的方法是冷却结晶;
⑤上述数据也可以说明,溶质的性质和温度能够影响物质的溶解性.
7.硫粉在氧气中燃烧产生火焰的颜色是( )
| A. | 黄色 | B. | 白色 | C. | 蓝紫色 | D. | 砖红色 |
4. 乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割成焊接金属,乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体.
乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割成焊接金属,乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体.
【查阅资料】电石主要成分为碳化钙(CaC2),它没有可燃性.
【提出问题】白色固体时什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:CaO;猜想二:CaCO3;猜想三:Ca(OH)2;他的依据是质量守恒定律.
【进行实验】
【交流反思】通过上述实验可知,电石在保护和运输时的注意事项防止与水接触.
 乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割成焊接金属,乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体.
乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割成焊接金属,乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体.【查阅资料】电石主要成分为碳化钙(CaC2),它没有可燃性.
【提出问题】白色固体时什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:CaO;猜想二:CaCO3;猜想三:Ca(OH)2;他的依据是质量守恒定律.
【进行实验】
| 实验步骤 | 实验现象及解释 | 结论 |
| (1)取少量白色固体于试管中,滴加稀盐酸 | 没有气泡 | 猜想二不成立 |
| (2)取少量白色固体加入水中,取上层清液,通入CO2 | 变浑浊,反应的方程式为 Ca(OH)2+CO2=CaCO3↓+H2O | 猜想三成立 |
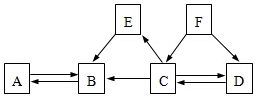 初中化学几种常见物质之间的相互转化关系如图所示.已知,常温下B、C为气体,且B是植物进行光合作用的一种重要原料;D、F均为无色液体,都由两种相同的元素组成,E是黑色固体,与稀硫酸反应得到蓝色溶液(部分反应物和生成物及反应条件已略去).回答下列相关的问题:
初中化学几种常见物质之间的相互转化关系如图所示.已知,常温下B、C为气体,且B是植物进行光合作用的一种重要原料;D、F均为无色液体,都由两种相同的元素组成,E是黑色固体,与稀硫酸反应得到蓝色溶液(部分反应物和生成物及反应条件已略去).回答下列相关的问题: