题目内容
20. 已知空气的主要成分是氮气和氧气,某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示:
已知空气的主要成分是氮气和氧气,某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示:(1)红磷在集气瓶中发生反应的文字表达式为磷+氧气$\stackrel{点燃}{→}$五氧化二磷,实验现象:红磷剧烈的燃烧,产生大量白烟.
(2)该实验中红磷稍过量,目的是将空气中氧气完全反应掉.
(3)待燃烧停止,白烟消失并冷却后,打开止水夹,观察到烧杯中的水进入集气瓶,瓶内水量约是集气瓶体积的,由本实验还可以推知氮气的哪一性质?试写出其中一种.
(4)若将红磷换成炭粉,该实验能否获得成功?否,理由是炭粉燃烧消耗氧气,同时生成二氧化碳气体,集气瓶内压强基本不变,水不倒流.
分析 本题是测定空气中氧气的含量,我们常用燃烧红磷或白磷的方法,因为磷燃烧生成白色固体五氧化二磷,几乎不占空间,使得内外产生气压差,从而得到正确的结论.因此在选择可燃物时,必须考虑到:燃烧的条件;生成物的状态;不与空气中其他物质发生反应.保证本实验成功的关键是:①装置气密性好;②红磷要足量;③要冷却至室温再读数.
解答 解:(1)实验中,红磷燃烧的现象是:红磷剧烈的燃烧,产生大量白烟;磷与氧气在点燃条件下反应生成五氧化二磷,该反应的文字表达式为:磷+氧气$\stackrel{点燃}{→}$五氧化二磷;
故答案为:磷+氧气$\stackrel{点燃}{→}$五氧化二磷;红磷剧烈的燃烧,产生大量白烟;
(2)该实验中红磷稍过量,目的是将空气中氧气完全反应掉;
故答案为:将空气中氧气完全反应掉;
(3)待燃烧停止,白烟消失并冷却后,打开止水夹,观察到现象为:水进入集气瓶,进入集气瓶中的水约占集气瓶容积的五分之一;由此可知氧气约占空气总体积的五分之一;由本实验还可推知氮气不溶于水,不能燃烧,不支持燃烧;
故填:$\frac{1}{5}$;不溶于水(或不能燃烧、不支持燃烧等);
(4)炭粉燃烧消耗氧气,同时生成二氧化碳气体,集气瓶内压强基本不变,水不倒流,故不能将红磷换成炭粉;
故填:否;炭粉燃烧消耗氧气,同时生成二氧化碳气体,集气瓶内压强基本不变,水不倒流.
点评 本考点考查了空气中氧气的含量的探究,并且注重了实验方案的评价,掌握用红磷测定空气组成的实验原理、操作、现象、结论和注意事项是解题的关键.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
15.在高温条件下,A、B两种物质可以发生化学反应生成C和D.反应前后分子种类变化的微观示意图如图所示.在这个化学反应中,以下叙述正确的是( )
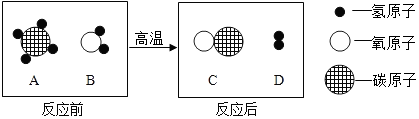

| A. | 该反应是置换反应 | B. | 物质B的相对分子质量是16 | ||
| C. | 生成C和D的微粒个数比1:1 | D. | 生成C和D的质量比是14:3 |
8. 实验室中某些气体的制取、干燥及收集装置如图所示(省略夹持和净化装置),仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )己知:浓盐酸遇到浓硫酸可以逸出氯化氢气体
实验室中某些气体的制取、干燥及收集装置如图所示(省略夹持和净化装置),仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )己知:浓盐酸遇到浓硫酸可以逸出氯化氢气体
 实验室中某些气体的制取、干燥及收集装置如图所示(省略夹持和净化装置),仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )己知:浓盐酸遇到浓硫酸可以逸出氯化氢气体
实验室中某些气体的制取、干燥及收集装置如图所示(省略夹持和净化装置),仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )己知:浓盐酸遇到浓硫酸可以逸出氯化氢气体| A | B | C | D | |
| a | 稀盐酸 | 稀硫酸 | 双氧水 | 浓疏酸 |
| b | 大理石 | 锌粒 | 二氧化锰 | 浓盐酸 |
| c | 固体氢氧化钠 | 碱石灰 | 固体氢氧化钠 | 碱石灰 |
| d | 二氧化碳 | 氢气 | 氧气 | 氯化氢 |
| A. | A | B. | B | C. | C | D. | D |

 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下: