题目内容
相同质量的SO2和SO3中氧元素质量比为 ,所含分子数之比为 .
考点:化合物中某元素的质量计算
专题:化学式的计算
分析:根据物质中某元素的质量分数=
×100%,设SO3和SO2的质量都是1g,分别计算SO3中氧的质量为与SO2中氧的质量,即可求出二者中氧的质量比,从而求得分子数之比.
| 该元素相对原子质量×原子个数 |
| 该物质的相对分子质量 |
解答:解:
(1)设SO3和SO2的质量都是1g,则:
SO3中氧元素的质量为:1g×
×100%=
g;
SO2中氧元素的质量为:1g×
×100%=
g.
SO2和SO3中,氧元素的质量比为
g:
g=5:6.
(2)相同质量的SO2和SO3中硫元素的质量比等于其分子个数比,故设SO3和SO2的质量都是1g,则:
SO3中硫元素的质量为:1g×
×100%=
g;
SO2中硫元素的质量为:1g×
×100%=
g.
SO2和SO3中,硫元素的质量比为
g:
g=5:4.
故答案为:6、5:4
(1)设SO3和SO2的质量都是1g,则:
SO3中氧元素的质量为:1g×
| 16×3 |
| 32+16×3 |
| 3 |
| 5 |
SO2中氧元素的质量为:1g×
| 16×2 |
| 32+16×2 |
| 1 |
| 2 |
SO2和SO3中,氧元素的质量比为
| 1 |
| 2 |
| 3 |
| 5 |
(2)相同质量的SO2和SO3中硫元素的质量比等于其分子个数比,故设SO3和SO2的质量都是1g,则:
SO3中硫元素的质量为:1g×
| 32 |
| 32+16×3 |
| 2 |
| 5 |
SO2中硫元素的质量为:1g×
| 32 |
| 32+16×2 |
| 1 |
| 2 |
SO2和SO3中,硫元素的质量比为
| 1 |
| 2 |
| 2 |
| 5 |
故答案为:6、5:4
点评:本题主要考查学生运用化学式进行计算的能力.学生需根据题意的要求,运用假设法,才能正确解答.

练习册系列答案
 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
如图是金刚石和石墨的结构示意图,它们的化学性质相似,物理性质却有很大差异.其原因是( )
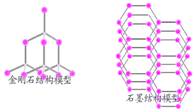

| A、碳原子结构不同 |
| B、石墨含有杂质 |
| C、碳原子的排列方式不同 |
| D、碳元素化合价不同 |
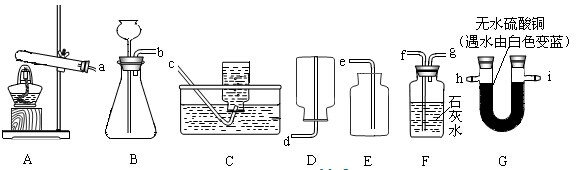

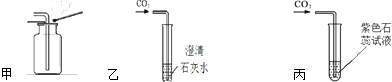
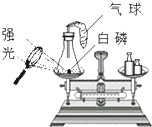 某化学兴趣小组利用如图装置进行质量守恒定律的探究.
某化学兴趣小组利用如图装置进行质量守恒定律的探究.