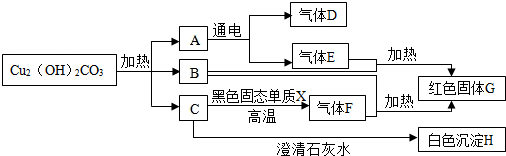
题目内容
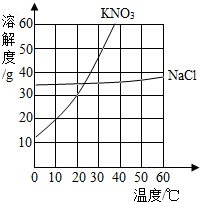 如图是硝酸钾和氯化钠的溶解度曲线.
如图是硝酸钾和氯化钠的溶解度曲线.(1)硝酸钾的溶解度随温度升高而
(2)要从氯化钠溶液中提取氯化钠,最好采用
(3)要使硝酸钾的饱和溶液变为不饱和溶液,除加水之外还可采用的方法是
(4)40℃时,饱和硝酸钾溶液的溶质质量分数比饱和氯化钠溶液的溶质质量分数(填“大”或“小”)
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,饱和溶液和不饱和溶液相互转变的方法,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)根据硝酸钾的溶解度曲线考虑;(2)根据氯化钠的溶解度随温度变化不大考虑;(3)根据饱和变为不饱和的方法考虑;(4)根据饱和溶液的溶质质量分数大小与溶解度有关考虑.
解答:解:(1)由硝酸钾的溶解度曲线可知,硝酸钾的溶解度随温度升高而增大;
(2)氯化钠的溶解度随温度变化不大,所以要从氯化钠溶液中提取氯化钠,最好采用蒸发溶剂的方法;
(3)饱和变为不饱和的常用方法:加入溶剂,改变温度,由于硝酸钾的溶解度随温度升高而增大,所以由饱和溶液变为不饱和溶液是升高温度;
(4)饱和溶液的溶质质量分数大小与溶解度有关,40℃时,硝酸钾的溶解度大于氯化钠的溶解度,所以40℃时,饱和硝酸钾溶液的溶质质量分数比饱和氯化钠溶液的溶质质量分数大.
故答案为:(1)增大;(2)蒸发溶剂;(3)升高温度;(4)大.
(2)氯化钠的溶解度随温度变化不大,所以要从氯化钠溶液中提取氯化钠,最好采用蒸发溶剂的方法;
(3)饱和变为不饱和的常用方法:加入溶剂,改变温度,由于硝酸钾的溶解度随温度升高而增大,所以由饱和溶液变为不饱和溶液是升高温度;
(4)饱和溶液的溶质质量分数大小与溶解度有关,40℃时,硝酸钾的溶解度大于氯化钠的溶解度,所以40℃时,饱和硝酸钾溶液的溶质质量分数比饱和氯化钠溶液的溶质质量分数大.
故答案为:(1)增大;(2)蒸发溶剂;(3)升高温度;(4)大.
点评:解答本题关键是要知道溶解度曲线的意义,溶质从溶液中结晶析出的方法,饱和溶液与不饱和溶液的相互转化方法,饱和溶液的溶质质量分数=
×100%
| 溶解度 |
| 100g+溶解度 |

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
现有A、B、C、D四种物质的化学反应关系如下表.且它们的相对分子质量之比是3:40:32:11,下面的说法中错误的是( )
| 物 质 | A | B | C | D |
| 反应前质量/g | 15 | 160 | 5 | 12 |
| 反应后质量/g | 待测 | 0 | 133 | 56 |
| A、完全反应后A的质量是3g |
| B、化学反应方程式中B与C的化学计量数的比是1:1 |
| C、该反应是化合反应 |
| D、该化学反应遵守质量守恒定律 |
下列物质中,属于纯净物的是( )
A、 加碘盐 |
B、 调和植物油 |
C、 沐浴液 |
D、 干冰 |


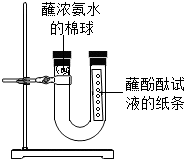 如图是有关分子性质的实验:在滤纸条上每隔2厘米处滴一滴无色酚酞试液,将滤纸条放入试管中,并在试管口塞上一团棉花.用滴管吸取浓氨水,将它滴在棉花上:
如图是有关分子性质的实验:在滤纸条上每隔2厘米处滴一滴无色酚酞试液,将滤纸条放入试管中,并在试管口塞上一团棉花.用滴管吸取浓氨水,将它滴在棉花上: