题目内容
用“>”或“<”或“=”填空:
(1)人体含钙量______人体含锌量.
(2)H2O2中氧元素的化合价______O3中氧元素的化合价.
(3)电解水实验中,正极产生气体体积______负极产生气体体积.
(4)一个水分子中含电子数______一个甲烷分子中含电子数.
(5)葡萄糖(C6H12O6)溶液中氢、氧元素质量比______水中氢、氧元素质量比.
解:(1)人体内含铁约为4~5g,含锌约为2.5g,故人体含钙量>人体含锌量;
(2)H2O2中氧元素的化合价为-1,O3中氧元素的化合价为0;
(3)正极产生氧气,负极产生氢气,为1:2的关系;
(4)一个水分子中含电子数 和一个甲烷分子中含电子数都是10个,故相等;
(5)葡萄糖(C6H12O6)溶液中氢、氧元素质量比和水中氢、氧元素质量比都是2:1,故相等;
故答案为:(1)>(2)<(3)<(4)=(5)=
分析:一些必需的微量元素对人体作用非常大,人体必需保证微量元素在人体的一定含量,如人体内含铁约为4~5g,含锌约为2.5g;摄入过多、过少都对健康产生影响.
点评:人体必需保证每天微量元素的摄取,如铁在人体内的含量约为4~5g,过多、过少都对健康不利.
(2)H2O2中氧元素的化合价为-1,O3中氧元素的化合价为0;
(3)正极产生氧气,负极产生氢气,为1:2的关系;
(4)一个水分子中含电子数 和一个甲烷分子中含电子数都是10个,故相等;
(5)葡萄糖(C6H12O6)溶液中氢、氧元素质量比和水中氢、氧元素质量比都是2:1,故相等;
故答案为:(1)>(2)<(3)<(4)=(5)=
分析:一些必需的微量元素对人体作用非常大,人体必需保证微量元素在人体的一定含量,如人体内含铁约为4~5g,含锌约为2.5g;摄入过多、过少都对健康产生影响.
点评:人体必需保证每天微量元素的摄取,如铁在人体内的含量约为4~5g,过多、过少都对健康不利.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
 17、(超市中的许多食物用保鲜膜包装后出售.保鲜膜为什么可以“保鲜”呢?
17、(超市中的许多食物用保鲜膜包装后出售.保鲜膜为什么可以“保鲜”呢?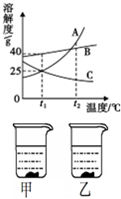 A、B、C三种固体物质的溶解度曲线如图所示.
A、B、C三种固体物质的溶解度曲线如图所示.