题目内容
国家质量标准规定:市售尿素中CO(NH2)2的质量分数在96%以上为达标一级品,现某化肥厂出售的一批尿素,其含氮量为42%(杂质不含氮),通过计算说明该尿素可否按一级品出售(写出计算过程).
考点:元素的质量分数计算
专题:化学式的计算
分析:根据题意,假设每袋尿素的质量为50kg,含氮量为42%,据此进行分析解答即可.
解答:解:根据题意,假设每袋尿素的质量为50kg,含氮量为42%,每袋商品尿素含氮元素的质量为50kg×42%=21kg.
每袋商品尿素含尿素的质量为21kg÷
×100%=45kg,每袋商品尿素含尿素的质量分数为:
×100%=90%;因为90%<96%,所以该尿素不可以按一级品出售.
答:该尿素不可以按一级品出售.
每袋商品尿素含尿素的质量为21kg÷
| 14×2 |
| 12+16+(14+1×2)×2 |
| 45kg |
| 50kg |
答:该尿素不可以按一级品出售.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
氧气可以和许多物质发生化学反应,如图所示,有关氧气的三个反应的叙述错误的是( )


| A、都是化合反应 |
| B、都是氧化反应 |
| C、生成物都是氧化物 |
| D、甲和丙实验时,瓶内放液体的目的是一样的 |
化学概念在逻辑上存在如图所示的关系,对下列概念间的关系说法正确的是( )

①纯净物与混合物属于包含关系
②化合物与氧化物属于包含关系
③单质与化合物属于交叉关系
④金属元素与分金属元素属于并列关系.

①纯净物与混合物属于包含关系
②化合物与氧化物属于包含关系
③单质与化合物属于交叉关系
④金属元素与分金属元素属于并列关系.
| A、①② | B、③④ | C、②④ | D、①④ |
将一定量的乙醇(C2H6O)和氧气置于一个封闭容器中引燃,充分反应,测得反应前后各物质质量如表.下列判断正确的是( )
| 物质 | 乙醇 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 4.6 | 8.0 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 5.4 | 4.4 | a |
| A、表中a的值为2.6 |
| B、X一定是该反应的催化剂 |
| C、X可能含有氢元素 |
| D、若反应前氧气的质量是9.6g,则a的值为0 |
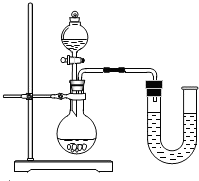


 水是生命之源,人类的日常生活与工农业生产都离不开水.小刚探究了水的组成(装置如图所示).通电一段时间后,试管1中所收集的气体为
水是生命之源,人类的日常生活与工农业生产都离不开水.小刚探究了水的组成(装置如图所示).通电一段时间后,试管1中所收集的气体为