题目内容
某学习小组同学用久置的过氧化氢溶液(如图)制取氧气,取2g二氧化锰于锥形瓶中,然后慢慢滴入34g过氧化氢溶液,充分反应。完成下列分析及计算:
(1)小明根据过氧化氢中氧元素的质量分数计算氧气的质量,其计算式为:
 生成氧气的质量=34g×10%×
生成氧气的质量=34g×10%× ×100%
×100%
=34g×10%× ×1
×1 00%=3.2g。
00%=3.2g。
老师指出小明的计算是错误的,你认为错误的原因是 ▲ f填字母序号)。
A.过氧化氢的氧元素的质量分数计算有误
B.过氧化氢中的氧元素没有全部转移到氧气中
(2)请你根据化学方程 式帮助小明计算理论上可制取氧气的质量。
式帮助小明计算理论上可制取氧气的质量。
(3)小亮思考:过氧化氢不稳定会自然分解,导致溶液中溶质的质量分数减小。实 验结束后,称得锥形瓶内剩余物质的总质量是35.2g。请计算这瓶过氧化氢溶液中实际溶质的质量分数。
验结束后,称得锥形瓶内剩余物质的总质量是35.2g。请计算这瓶过氧化氢溶液中实际溶质的质量分数。
略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 某学习小组同学用久置的过氧化氢溶液(如图)制取氧气,取2g二氧化锰于锥形瓶中,然后慢慢滴入34g过氧化氢溶液,充分反应.完成下列分析及计算:
某学习小组同学用久置的过氧化氢溶液(如图)制取氧气,取2g二氧化锰于锥形瓶中,然后慢慢滴入34g过氧化氢溶液,充分反应.完成下列分析及计算:
 ×100%=3.2g。
×100%=3.2g。
 ×100%=3.2g。
×100%=3.2g。 ×100%=34g×10%×
×100%=34g×10%× ×100%=3.2g.
×100%=3.2g.

 ×100%
×100%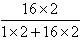 ×100%=3.2g。
×100%=3.2g。