题目内容
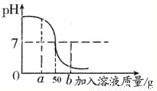
 向盛有45g蒸馏水的烧杯中加入含氯化钠的氢氧化钠的固体混合物5g,使之全部溶解后,向烧杯中滴加溶质质量分数为7.3%的稀盐酸,它们反应中溶液的pH与加入稀盐酸溶液的质量关系如图所示.请回答和计算下列问题:
向盛有45g蒸馏水的烧杯中加入含氯化钠的氢氧化钠的固体混合物5g,使之全部溶解后,向烧杯中滴加溶质质量分数为7.3%的稀盐酸,它们反应中溶液的pH与加入稀盐酸溶液的质量关系如图所示.请回答和计算下列问题:(1)当加入稀盐酸的质量为ag时,向所得溶液中滴加酚酞试液,溶液呈
红
红
色,此时所得溶液中存在的微粒有(填符号)Na+、OH-、Cl-、H2O
Na+、OH-、Cl-、H2O
.当加入稀盐酸的质量为bg时,所得溶液中的溶质为NaCl、HCl
NaCl、HCl
(写化学式)(2)原固体混合物中钠元素的质量分数?
(3)当加入稀盐酸的质量为50g时所得溶液中溶质的质量分数?
分析:(1)氢氧化钠溶液呈碱性,从图中分析可以知道在a点时溶液仍呈碱性,所以此时加入酚酞试液,会变红,而此时溶液中含有氢氧化钠、水和氯化钠;当到达b点时,溶液呈酸性,此时盐酸过过量,所含的溶质为氯化钠和氯化氢,可以据此解答该题;
(2)从图中分析可以知道50g盐酸与氢氧化钠溶液恰好完全反应,所以可以根据化学方程式求算出氢氧化钠的质量,进而求算出混合物中氯化钠的质量,即可然后求算出钠元素的质量,即可完成解答;
(3)根据(2)的分析可以知道反应后的溶液为氯化钠的溶液,所以可以据此结合化学方程式完成解答.
(2)从图中分析可以知道50g盐酸与氢氧化钠溶液恰好完全反应,所以可以根据化学方程式求算出氢氧化钠的质量,进而求算出混合物中氯化钠的质量,即可然后求算出钠元素的质量,即可完成解答;
(3)根据(2)的分析可以知道反应后的溶液为氯化钠的溶液,所以可以据此结合化学方程式完成解答.
解答:解:(1)氢氧化钠溶液呈碱性,从图中分析可以知道在a点时溶液仍呈碱性,所以此时加入酚酞试液,会变红,而此时溶液中含有氢氧化钠、水和氯化钠,它们可以解离出:Na+、OH-、Cl-、H2O;当到达b点时,溶液呈酸性,此时盐酸过过量,所含的溶质为氯化钠和氯化氢;
(2)当加入稀盐酸的质量为50g时,氢氧化钠已被恰好完全反应,此时消耗的盐酸中氯化氢的质量为:50g×7.3%=3.65g
设原混合物中氢氧化钠的质量为x,反应完全后生成氯化钠的质量为y
HCl+NaOH═NaCl+H2O
36.5 40 58.5
3.65g x y
=
=
解得:x=4g,y=5.85g
所以氯化钠的质量为:5g-4g=1g,
反应后所得溶液中氯化钠的质量为:5.85g+1g=6.85g;
根据质量守恒定律可以知道反应前后钠元素的质量不变,所以氯化钠中钠元素的质量和混合物中钠元素的质量相等,
故钠元素的质量分数为:
×100%=53.8%;
(3)反应后所得溶液的质量分数为:
×100%=6.85%.
答:(2)原固体混合物中钠元素的质量分数为53.8%;
(3)当加入稀盐酸的质量为50g时所得溶液中溶质的质量分数6.85%.
故答案为:(1)红色;Na+、OH-、Cl-、H2O;NaCl、HCl;
(2)53.8%;
(3)6.85%.
(2)当加入稀盐酸的质量为50g时,氢氧化钠已被恰好完全反应,此时消耗的盐酸中氯化氢的质量为:50g×7.3%=3.65g
设原混合物中氢氧化钠的质量为x,反应完全后生成氯化钠的质量为y
HCl+NaOH═NaCl+H2O
36.5 40 58.5
3.65g x y
| 36.5 |
| 3.65g |
| 40 |
| x |
| 58.5 |
| y |
解得:x=4g,y=5.85g
所以氯化钠的质量为:5g-4g=1g,
反应后所得溶液中氯化钠的质量为:5.85g+1g=6.85g;
根据质量守恒定律可以知道反应前后钠元素的质量不变,所以氯化钠中钠元素的质量和混合物中钠元素的质量相等,
故钠元素的质量分数为:
6.85g×
| ||
| 5g |
(3)反应后所得溶液的质量分数为:
| 6.85g |
| 45g+5g+50g |
答:(2)原固体混合物中钠元素的质量分数为53.8%;
(3)当加入稀盐酸的质量为50g时所得溶液中溶质的质量分数6.85%.
故答案为:(1)红色;Na+、OH-、Cl-、H2O;NaCl、HCl;
(2)53.8%;
(3)6.85%.
点评:本题主要考查学生运用化学方程式和溶质质量分数公式进行计算的能力.解题时要注意解题步骤的规范性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
我们知道氧气是人体生命所必需的,在一般情况下,人可以呼吸空气中的氧气,但在特殊情况下,如在核潜艇里工作的人员,如何获得氧气呢?研究表明用“金属过氧化物处理系统”使氧“再生”具有良好的实际应用价值.
已知:淡黄色的过氧化钠固体在常温下即能与二氧化碳反应生成氧气
反应方程式为:2Na2O2+2CO2═2Na2CO3+O2
(1)你认为用这种方法制氧气的优点是 ;
(2)小明欲探究过氧化钠吸收和释放的气体之间体积关系以及反应的热效应,设计实验如下,请回答下列相关问题:
①简述检查装置气密性的方法 ;
②向U形管内盛装过量的Na2O2药品,注射器中为二氧化碳气体,连接好装置.药品为什么需过量 ;
③缓缓推动注射器A活塞,片刻,可以观察到温度计液柱明显上升,说明反应 (填“吸热”或“放热”)同时还可以观察到固体粉末发生变化的现象是 ;
④小明查阅资料得知:相同的条件下,相同体积的气体具有相等的分子数,则待A注射器中二氧化碳气体反应完全后,装置恢复至常温,B注射器中活塞应停留在 mL处.(不考虑实验带来的误差)
(3)Na2O2露置在空气中容易发生变质,如何检验已经变质,简述方法、现象和结论.
变质的程度如何呢?部分同学对“已部分变质的Na2O2(含Na2CO3)的纯度测定”设计了实验,步骤如下:
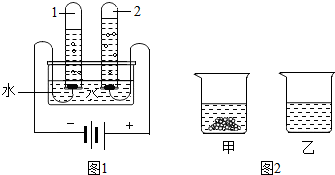
①按图(1)连接装置,并检查气密性;②准确称得盛有碱石灰的干燥管D的质量为w1g;③准确称得mg样品放入容器b中;④打开a,缓缓滴入稀硫酸,至不再产生气泡为止;⑤打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为w2g;⑥根据D装置质量差进行计算.试回答:
i写出盛放稀硫酸的实验仪器名称 ;
ii若④⑤两步的实验操作太快,则会导致测定的Na2O2的纯度 (填“偏大”或“偏小”).
iii鼓入空气的目的是 ,装置A中试剂X应选用 ;
ivE装置的作用是 ;
(4)小红同学通过查阅资料了解到Na2O2还能与水反应,方程式为:2Na2O2+2H2O═4NaOH+O2↑于是她根据这一原理设计了另一种测定Na2O2的纯度的方法:①称取20g样品于一只质量为45g的锥形中;②一次性加入20mL蒸馏水后将锥形瓶放置在电子天平上,观察显示数字的变化,并记录(数据见下表);③进行计算.
i从上表数据判断, 秒时,已经反应完全;
ii请你帮小红同学计算此样品中Na2O2的纯度,并写出过程.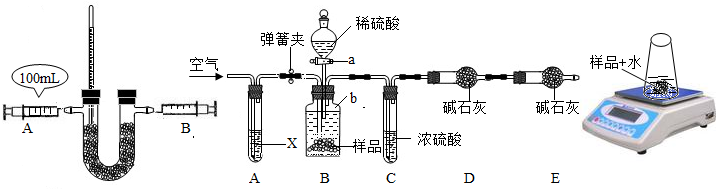
已知:淡黄色的过氧化钠固体在常温下即能与二氧化碳反应生成氧气
反应方程式为:2Na2O2+2CO2═2Na2CO3+O2
(1)你认为用这种方法制氧气的优点是
(2)小明欲探究过氧化钠吸收和释放的气体之间体积关系以及反应的热效应,设计实验如下,请回答下列相关问题:
①简述检查装置气密性的方法
②向U形管内盛装过量的Na2O2药品,注射器中为二氧化碳气体,连接好装置.药品为什么需过量
③缓缓推动注射器A活塞,片刻,可以观察到温度计液柱明显上升,说明反应
④小明查阅资料得知:相同的条件下,相同体积的气体具有相等的分子数,则待A注射器中二氧化碳气体反应完全后,装置恢复至常温,B注射器中活塞应停留在
(3)Na2O2露置在空气中容易发生变质,如何检验已经变质,简述方法、现象和结论.
变质的程度如何呢?部分同学对“已部分变质的Na2O2(含Na2CO3)的纯度测定”设计了实验,步骤如下:
①按图(1)连接装置,并检查气密性;②准确称得盛有碱石灰的干燥管D的质量为w1g;③准确称得mg样品放入容器b中;④打开a,缓缓滴入稀硫酸,至不再产生气泡为止;⑤打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为w2g;⑥根据D装置质量差进行计算.试回答:
i写出盛放稀硫酸的实验仪器名称
ii若④⑤两步的实验操作太快,则会导致测定的Na2O2的纯度
iii鼓入空气的目的是
ivE装置的作用是
(4)小红同学通过查阅资料了解到Na2O2还能与水反应,方程式为:2Na2O2+2H2O═4NaOH+O2↑于是她根据这一原理设计了另一种测定Na2O2的纯度的方法:①称取20g样品于一只质量为45g的锥形中;②一次性加入20mL蒸馏水后将锥形瓶放置在电子天平上,观察显示数字的变化,并记录(数据见下表);③进行计算.
| 时间/s | 60 | 120 | 180 | 240 | 300 |
| 天平示数/g | 83.82 | 82.43 | 82.15 | 81.80 | 81.80 |
ii请你帮小红同学计算此样品中Na2O2的纯度,并写出过程.

 (2013?房山区一模)水和溶液在生命活动和生产、生活中起着十分重要的作用.
(2013?房山区一模)水和溶液在生命活动和生产、生活中起着十分重要的作用.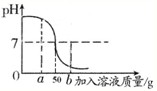 向盛有45g蒸馏水的烧杯中加入含氯化钠的氢氧化钠的固体混合物5g,使之全部溶解后,向烧杯中滴加溶质质量分数为7.3%的稀盐酸,它们反应中溶液的pH与加入稀盐酸溶液的质量关系如图所示.请回答和计算下列问题:
向盛有45g蒸馏水的烧杯中加入含氯化钠的氢氧化钠的固体混合物5g,使之全部溶解后,向烧杯中滴加溶质质量分数为7.3%的稀盐酸,它们反应中溶液的pH与加入稀盐酸溶液的质量关系如图所示.请回答和计算下列问题: