题目内容
56 g10%的氢氧化钾溶液中加入一定量的稀硫酸,恰好完全反应后所得溶液质量为80.5 g,计算所用稀硫酸的溶质质量分数。
解:设所用稀硫酸溶质的质量为x
氢氧化钾质量=56 g×10%=5.6 g 1分
H2SO4 +2KOH K2SO4 + 2H2O
98 112
x 5.6 g
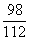 =
=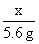
x=4.9 g 1分
稀硫酸溶液的质量=80.5 g-56 g=24.5 g 1分
所用稀硫酸溶质的质量分数=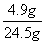 ×100%=20% 1分
×100%=20% 1分
答:所用稀硫酸溶质的质量分数为20%。

练习册系列答案
相关题目
 实验室有一瓶氢氧化钾浓溶液,瓶上标签内容如图所示,请你根据签上提供的数据解答下列问题:
实验室有一瓶氢氧化钾浓溶液,瓶上标签内容如图所示,请你根据签上提供的数据解答下列问题: