题目内容
将铜和氧化铜固体混合物粉末9.6g放入烧杯中,当加入稀硫酸152g时,氧化铜与硫酸恰好完全反应,过滤,烘干,得滤渣1.6g.(1)混合物中铜元素的质量分数为______(结果保留一位小数点).
(2)通过计算求反应后所得溶液中溶质的质量分数.
【答案】分析:利用氧化铜能与硫酸反应而铜不能,所以滤渣即为铜的质量,据此可求氧化铜的质量,以此为突破口分析解答即可;
解答:解:(1)氧化铜能与硫酸反应而铜不能,所以滤渣即为铜的质量,因此氧化铜的质量是9.6g-1.6g=8g,故原混合物中铜元素的质量为8g×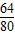 +1.6g=8g,所以混合物中铜元素的质量分数为
+1.6g=8g,所以混合物中铜元素的质量分数为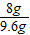 ×100%=83.3%
×100%=83.3%
(2)设生成的硫酸铜质量是x
CuO+H2SO4=CuSO4+H2O
80 160
8g x
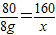
x=16g
反应后所得溶液中溶质的质量分数为: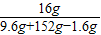 ×100%=10%
×100%=10%
故答案为:(1)83.3%;(2)反应后所得溶液中溶质的质量分数为10%;
点评:本题主要考查有关化学式的计算、含杂质物质的化学方程式计算,难度较大需要充分利用相关的计算知识.
解答:解:(1)氧化铜能与硫酸反应而铜不能,所以滤渣即为铜的质量,因此氧化铜的质量是9.6g-1.6g=8g,故原混合物中铜元素的质量为8g×
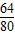 +1.6g=8g,所以混合物中铜元素的质量分数为
+1.6g=8g,所以混合物中铜元素的质量分数为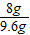 ×100%=83.3%
×100%=83.3%(2)设生成的硫酸铜质量是x
CuO+H2SO4=CuSO4+H2O
80 160
8g x
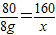
x=16g
反应后所得溶液中溶质的质量分数为:
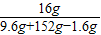 ×100%=10%
×100%=10%故答案为:(1)83.3%;(2)反应后所得溶液中溶质的质量分数为10%;
点评:本题主要考查有关化学式的计算、含杂质物质的化学方程式计算,难度较大需要充分利用相关的计算知识.

练习册系列答案
相关题目
 类比法是化学研究物质的重要方法之一.草酸的化学性质与碳酸相似.已知碳酸易分解,草酸在受热条件下也分解,仅生成三种氧化物.某校研究性学习小组对此展开探究:
类比法是化学研究物质的重要方法之一.草酸的化学性质与碳酸相似.已知碳酸易分解,草酸在受热条件下也分解,仅生成三种氧化物.某校研究性学习小组对此展开探究: (2012?大兴区二模)孔雀石主要成分是碱式碳酸铜[Cu2(OH)2CO3],绿色并具有浓淡的条状花纹(见右图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料.某校课外小组同学欲在实验室验证碱式碳酸铜制铜的反应原理.
(2012?大兴区二模)孔雀石主要成分是碱式碳酸铜[Cu2(OH)2CO3],绿色并具有浓淡的条状花纹(见右图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料.某校课外小组同学欲在实验室验证碱式碳酸铜制铜的反应原理. 类比法是化学研究物质的重要方法之一.草酸的化学性质与碳酸相似.已知碳酸易分解,草酸在受热条件下也分解,仅生成三种氧化物.某校研究性学习小组对此展开探究:
类比法是化学研究物质的重要方法之一.草酸的化学性质与碳酸相似.已知碳酸易分解,草酸在受热条件下也分解,仅生成三种氧化物.某校研究性学习小组对此展开探究:
