题目内容
6.尿素是一种常用的化肥,工业上生产尿素的反应的微观示意图如图: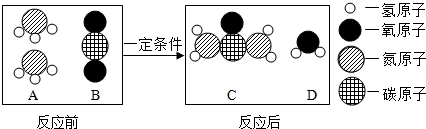
(1)反应前后各物质中属于氧化物的是BD(用A、B、C、D填空).
(2)物质C的一个分子中,含有8个原子.
(3)物质A中,氢元素的质量分数为17.6%(精确到0.1%).
(4)工业上生产尿素的化学方程式为2NH3+CO2=CO(NH2)2+H2O.
(5)该反应中A与D的质量比为17:9.
分析 由氧元素和另外一种元素组成的化合物是氧化物;
根据物质的微观粒子可以判断每个分子中含有的原子个数;
根据物质的化学式可以计算组成元素的质量分数;
根据微观粒子示意图可以书写反应的化学方程式;
根据反应的化学方程式可以计算物质之间的质量比.
解答 解:(1)反应前后各物质中属于氧化物的是B和D,B是二氧化碳,D是水,二氧化碳和水都是由氧元素和另外一种元素组成的化合物,都属于氧化物.
故填:BD.
(2)物质C的化学式是CO(NH2)2,一个分子中,含有,8个原子.
故填:8.
(3)物质A是氨气,化学式是NH3,氢元素的质量分数为:$\frac{3}{17}$×100%=17.6%.
故填:17.6%.
(4)工业上生产尿素的化学方程式为:2NH3+CO2=CO(NH2)2+H2O.
故填:2NH3+CO2=CO(NH2)2+H2O.
(5)该反应中A与D的质量比为:(17×2):18=17:9.
故填:17:9.
点评 本题主要考查根据示意图进行各方面判断的能力,要注意观察图中信息,从而进行正确解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.中国科学家屠呦呦因研究青蒿素而获2015年诺贝尔生理学或医学奖.青蒿素是从复合花序植物黄花蒿(即中药青蒿)中提取得到的一种无色针状晶体,是继乙氨嘧啶、氯喹、伯喹之后最有效的抗疟特效药;曾被世界卫生组织称做是“世界上唯一有效的疟疾治疗药物”.其分子式为C15H22O5.下列说法正确的是( )
| A. | 青蒿素是有15个碳原子、22个氢原子、5个氧原子构成的 | |
| B. | 青蒿素的相对分子质量为282g | |
| C. | 青蒿素中碳、氢元素质量比为15:22 | |
| D. | 青蒿素由碳、氢、氧三种元素组成 |
14.现有下列实验装置,请回答下列问题:
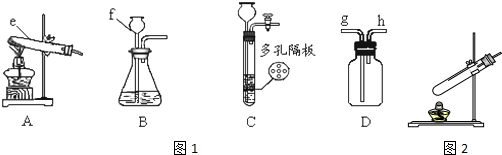
(1)图1中e、f仪器的名称:e试管,f长颈漏斗
(2)用氯酸钾和二氧化锰固体制氧气,选用的发生装置是A(填字母A、B、C、D),反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)用块状固体和液体不加热制取气体时,改用C装置(多孔隔板用来放块状固体)代替B装置的优点是随开随用、随关随停,容易控制.
(4)实验室里用双氧水和二氧化锰反应制氧气的化学反应方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该实验不能(填“能”或“不能”)选用C装置,若用D装置来收集生成的氧气,气体应从g(填g或h)通入.
(5)同学们想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
a.实验3中,加入的二氧化锰质量为5g.
b.相同条件下,实验3(填实验编号)产生氧气的速率最快,说明双氧水的溶质质量分数越大反应速率越快.
(6)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,同学分析原因后,采用了排水集气法收集气体,再检验,证明加热双氧水也可产生氧气.

(1)图1中e、f仪器的名称:e试管,f长颈漏斗
(2)用氯酸钾和二氧化锰固体制氧气,选用的发生装置是A(填字母A、B、C、D),反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)用块状固体和液体不加热制取气体时,改用C装置(多孔隔板用来放块状固体)代替B装置的优点是随开随用、随关随停,容易控制.
(4)实验室里用双氧水和二氧化锰反应制氧气的化学反应方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该实验不能(填“能”或“不能”)选用C装置,若用D装置来收集生成的氧气,气体应从g(填g或h)通入.
(5)同学们想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
| 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 5 | 67 |
b.相同条件下,实验3(填实验编号)产生氧气的速率最快,说明双氧水的溶质质量分数越大反应速率越快.
(6)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,同学分析原因后,采用了排水集气法收集气体,再检验,证明加热双氧水也可产生氧气.
1.在H2O2、SO2、CO2 三种物质中,都含有( )
| A. | 氧分子 | B. | 阳离子 | ||
| C. | 相同的氧原子个数 | D. | 氧元素 |
11.下列化学方程式书写正确的是( )
| A. | 4Fe+3O2$\stackrel{点燃}{→}$2Fe2O3 | B. | 2Mg+CO2$\stackrel{点燃}{→}$2MgO+C | ||
| C. | 2Fe+6HCl→FeCl3+3H2↑ | D. | CaCO3$\stackrel{高温}{→}$CaO+H2O |
6.下列物质属于纯净物的是( )
| A. | 黄铜 | B. | 干冰 | C. | 生铁 | D. | 不锈钢 |
7.下列对于意外事故的预防或处理错误的是( )
| 选项 | 意外事故 | 预防或处理方法 |
| A | 试管中的液体暴沸 | 立即将试管从酒精灯火焰上移开 |
| B | 不慎将燃着的酒精灯碰倒, 洒出的酒精在桌上燃烧 | 应立刻用湿抹布或沙扑盖 |
| C | 浓硫酸不慎溅到皮肤上 | 先用干布拭去,然后用大量水冲洗, 再涂上3%~5%的小苏打溶液 |
| D | 碱液不慎洒在衣服上 | 用水冲洗后,再涂上硫酸溶液 |
| A. | A | B. | B | C. | C | D. | D |