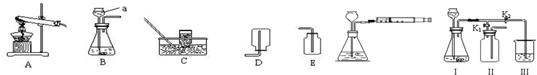
题目内容
某化学研究性学习小组在学习碱的化学性质时,设计了实验方案,进行了如图所示的实验,并查阅资料得知:Na2CO3溶液和澄清的石灰水都呈碱性(pH>7),CaCl2溶液呈中性(pH=7).
(1)甲实验中,滴有酚酞的氢氧化钠溶液呈 色,逐滴加入稀盐酸,直至溶液恰好呈无色为止.
(2)乙实验试管内产生白色沉淀,其发生反应的化学方程式为 .
(3)实验结束后,同学们将甲、乙两个实验的废液倒入同一个烧杯中,观察到废液呈浑浊并显红色,由此分析可知:
①废液中除碳酸钙、氯化钠、水和指示剂外,一定还含有 .
②依据上述实验过程,你认为引起废液呈碱性的物质组成共有 种可能.
(4)如果将乙实验中的澄清石灰水改为CaCl2溶液,同样进行实验(1)(2)(3)的操作,废液呈浑浊并显红色的现象 (填“可能”或“不可能”)出现.

| 根据已有的知识进行分析,酚酞试液在碱性溶液中为红色;氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,碳酸钠和氢氧化钙反应时可能是恰好完全反应,也可能是物质有剩余;氯化钙能与碳酸钠反应生成氯化钠和碳酸钙,同样存在物质过量的情况,据此解答. | |
| 解答: | 解:(1)氢氧化钠溶液呈碱性,能使酚酞试液变红,故填:红; (2)碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,故填:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH; (3)①酚酞试液在碱性溶液中为红色,由于碳酸钠与氢氧化钙反应生成氢氧化钠,故一定含有氢氧化钠,故填:氢氧化钠; ②若碳酸钠与氢氧化钙恰好完全反应,则可以是碳酸钙、氯化钠、水和指示剂以及氢氧化钠;若碳酸钠有剩余,则可以是碳酸钙、氯化钠、水、指示剂、氢氧化钠和碳酸钠;若是氢氧化钙有剩余,则可以是碳酸钙、氯化钠、水指示剂、氢氧化钠和氢氧化钙,故有三种物质组合,故填:3; (4)改成氯化钙溶液,若碳酸钠有剩余,由于碳酸钠溶液呈碱性,同样可能会出现溶液变浑浊的现象,故填:可能. |

 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案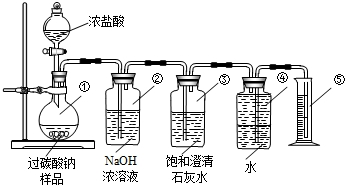
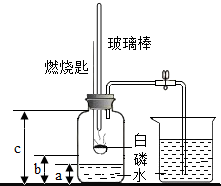 某化学研究性学习小组在学习了“空气中氧气含量测定”实验的基础上,改进了教材中的实验,设计出如图所示的实验装置.
某化学研究性学习小组在学习了“空气中氧气含量测定”实验的基础上,改进了教材中的实验,设计出如图所示的实验装置.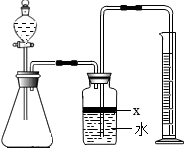 氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,某化学研究性学习小组设计并完成了如下实验.
氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,某化学研究性学习小组设计并完成了如下实验.