题目内容
图为甲乙两物质的溶解度曲线,下列说法正确的是( )
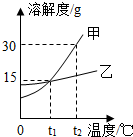

| A、要使接近饱和的乙溶液转化为饱和溶液,可以采用蒸发溶剂的方法 |
| B、甲的溶解度大于乙的溶解度 |
| C、t2℃时,可以配制成30%的甲溶液 |
| D、t1℃时,甲、乙两物质饱和溶液中溶质的质量分数均为15% |
考点:固体溶解度曲线及其作用,饱和溶液和不饱和溶液相互转变的方法,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:A、根据不饱和溶液变为饱和溶液的方法考虑;
B、根据溶解度大小比较方法考虑;
C、t2℃时根据饱和溶液溶质质量分数的计算方法考虑;
D、根据t1℃时甲、乙两物质的溶解度相等来解答;
B、根据溶解度大小比较方法考虑;
C、t2℃时根据饱和溶液溶质质量分数的计算方法考虑;
D、根据t1℃时甲、乙两物质的溶解度相等来解答;
解答:解:
A、要使接近饱和的乙溶液转化为饱和溶液,可以用蒸发溶剂或降低温度,故A正确;
B、比较溶解度大小必须有温度限制,故B错;
C、t2℃甲物质的溶解度使30g,饱和溶液的溶质质量分数为
×100g=23%,故C错;
D、t1℃时甲、乙两物质的溶解度是15g,饱和溶液的溶质质量分数相等,即
×100%=13%,故D错.
答案:A.
A、要使接近饱和的乙溶液转化为饱和溶液,可以用蒸发溶剂或降低温度,故A正确;
B、比较溶解度大小必须有温度限制,故B错;
C、t2℃甲物质的溶解度使30g,饱和溶液的溶质质量分数为
| 30g |
| 100g+30g |
D、t1℃时甲、乙两物质的溶解度是15g,饱和溶液的溶质质量分数相等,即
| 15g |
| 100g+15g |
答案:A.
点评:解答本题关键是要知道比较溶解度大小必须有温度限制,饱和溶液溶质质量分数计算与溶解度有关,知道不饱和溶液变为饱和溶液的方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
如图所示装置是某同学进行空气中氧气含量的实验探究.实验时烧杯中的水为500mL(图1),实验结束后烧杯的水为350mL(图2),然后,将烧杯内剩余的水倒入集气瓶并塞上双孔塞,水恰好满瓶(500mL).对这种现象解释合理的是( )


| A、红磷的量不足,瓶内氧气没有消耗完 |
| B、没等集气瓶冷却,就打开止水夹 |
| C、没有塞紧瓶塞,红磷熄灭冷却时外界空气进入瓶内 |
| D、点燃红磷后燃烧匙插入集气瓶慢,塞紧瓶塞之前,瓶内部分空气受热逸出 |
下列做法中,正确的是( )
| A、尝药品的味道 |
| B、用剩的药品放回原试剂瓶中 |
| C、使用天平时可用手直接拿砝码 |
| D、给装有固体药品的试管加热时,试管口略向下倾斜 |
下列各组物质混合后,可形成溶液的是( )
| A、石灰水与CO2 |
| B、植物油与汽油 |
| C、豆浆与水 |
| D、面粉与水 |
除去乙烷气体中混有的乙烯,最好的方法( )
| A、加入氢气与乙烯反应 |
| B、点燃 |
| C、通入适量溴水 |
| D、通过KMnO4溶液 |
根据实验操作所绘制的图象中,正确的是( )
A、 如图是石灰石和稀盐酸反应,固体剩余物的质量与产生气体的质量关系 |
B、 如图是一定温度下,向饱和硝酸钾溶液中不断加入硝酸钾固体,充分搅拌 |
C、 如图是向等质量、等质量分数的稀硫酸中分别加入过量的金属镁与铝,加入金属质量与产生氢气质量的关系 |
D、 如图是向一定质量铁粉中加入硫酸铜溶液,加入硫酸铜溶液与形成溶液总质量的关系 |
下列实验现象描述正确的是( )
| A、白磷自燃产生大量的白烟 |
| B、硫在空气中燃烧,产生明亮的蓝紫色火焰 |
| C、木炭在氧气中剧烈燃烧,放出大量的热,产生二氧化碳气体 |
| D、细铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 |