题目内容
1.食品吸潮和吸氧后容易变质,为了延长食品保质期.通常在包装袋中加入1小包干燥剂.某化学兴趣小组经过查阅资料,发现常见的食品干燥剂主要有两种:一种是以生石灰为主要成份的干燥剂(简称A类,下同);另一种是以硅胶为主要成份的干燥剂(简称B类,下同).请问答下列问题:(1)将装有A类干燥剂的小纸袋打开露置于潮湿的空气中,发现纸袋发热,与其发生反应的化学方程式CaO+H2O═Ca(OH)2.
(2)B类干燥剂中硅胶的主要成分为SiO2•nH2O.SiO2是氧化物 (填“酸”、“碱”、“盐”、“氧化物”).
(3)小组在查阅资料中,还发现了-种新型的食品干燥剂:泡沫铁粉(铁粉包裹在泡沫塑料中).当它露置于潮湿的空气中,很快变成铁锈(主要成分为Fe2O3•nH2O),并有发热现象,说明化学反应除了生成新物质外,还伴随着热量的变化.
分析 (1)一种是以生石灰为主要成份的干燥剂,简称A类,结合生石灰与水反应生成氢氧化钙,进行分析解答.
(2)根据SiO2是由硅元素和氧元素组成的化合物,进行分析解答.
(3)根据题意,泡沫铁粉(铁粉包裹在泡沫塑料中).当它露置于潮湿的空气中,很快变成铁锈(主要成分为Fe2O3•nH2O),并有发热现象,进行分析解答.
解答 解:(1)一种是以生石灰为主要成份的干燥剂,简称A类,生石灰与水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2.
(2)SiO2是由硅元素和氧元素组成的化合物,属于氧化物.
(3)泡沫铁粉(铁粉包裹在泡沫塑料中).当它露置于潮湿的空气中,很快变成铁锈(主要成分为Fe2O3•nH2O),并有发热现象,说明化学反应除了生成新物质外,还伴随着热量的变化.
故答案为:(1)CaO+H2O═Ca(OH)2;(2)氧化物;(3)热量的.
点评 本题难度不大,掌握生石灰的化学性质、酸碱盐与氧化物的特征、化学变化中的能量变化等是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列实验操作容易引发安全事故的是( )
| A. | 点燃可燃性气体前,先验纯 | |
| B. | 酒精灯着火,用水浇灭 | |
| C. | 加热固体时,试管口略向下倾斜 | |
| D. | 加热液体时,液体体积不超过试管容积的$\frac{1}{3}$ |
16.请你填写下表中的空白处:
(1)核电荷数(x).质子数(Y).电子数(z)之间的关系是x=Y=z;(符号表示)
(2)质子数(A).中子数(B)与相对原子质量(C)之间的关系是C=A+B;(符号表示)
(3)所有的原子中都含有质子和电子两种粒子.
(4)有一种特殊的原子是氢原子,其特殊之处是原子核内没有中子.
| 原子种类 | 核电荷数 | 质子数 | 中子数 | 核外电子数 | 相对原子质量 |
| 氢 | 1 | 0 | 1 | 1 | |
| 碳 | 6 | 6 | 6 | 6 | |
| 氧 | 8 | 8 | 8 | 8 | 16 |
| 钠 | 11 | 11 | 12 | 11 | 23 |
(2)质子数(A).中子数(B)与相对原子质量(C)之间的关系是C=A+B;(符号表示)
(3)所有的原子中都含有质子和电子两种粒子.
(4)有一种特殊的原子是氢原子,其特殊之处是原子核内没有中子.
6.某学生用量筒取液体时,量筒平稳地放置在实验台上,使视线同溶液凹液面的最低点保持水平,读数为18mL;倒出部分液体后,俯视凹面的最低处,读数为12mL,则该学生实际倒出的液体体积为( )
| A. | 可能大于也可能小于6mL | B. | 小于6mL | ||
| C. | 等于6mL | D. | 大于6mL |
10.防止铁腐蚀可以进行烤蓝,发生的反应是3Fe+4H2O $\frac{\underline{\;高温\;}}{\;}$ M+4H2↑,则M的化学式为( )
| A. | FeO | B. | Fe(OH)2 | C. | Fe2O3 | D. | Fe3O4 |
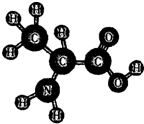 蛋白质是人类重要的营养物质,它是由多种氨基酸构成的化合物,丙氨酸是其中的一种.如图是丙氨酸分子的结构模型,请回答下列问题:
蛋白质是人类重要的营养物质,它是由多种氨基酸构成的化合物,丙氨酸是其中的一种.如图是丙氨酸分子的结构模型,请回答下列问题: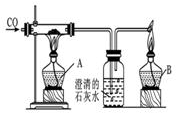 如图是用赤铁矿(主要成分氧化铁)炼铁原理的装置图:
如图是用赤铁矿(主要成分氧化铁)炼铁原理的装置图: