题目内容
20.元素周期表使化学学习有规律可循,请认真分析并回答下列问题.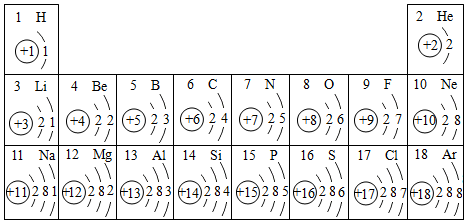
(1)原子序数为12 的元素位于周期表中第三周期,它属于金属(填“金属”或“非金属”)元素.
(2)在化学反应中,原子序数为16 的元素的原子容易得到(填“得到”或“失去”)电子,所形成的粒子的符号是S2-.
(3)由图分析:与氯元素的化学性质相似的元素是氟或F.
(4)同周期元素,从左到右,各元素原子随原子序数的增加最外层电子数,增加.
(5)11 号和17 号元素组成的物质由Na+、Cl-.(填粒子符号)构成.
分析 (1)根据原子核外的电子层数等于其所在周期数以及元素的分类来分析;
(2)原子序数为16的原子核内质子数为16;若最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子;
(3)根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,进行分析解答;
(4)根据元素周期表的规律来分析.
(5)电荷数分别为11和17的元素为钠元素和氯元素,组成的化合物为氯化钠,可以据此解答该题;
解答 解:(1)12号元素是镁元素,其原子核外有3个电子层,所以在元素周期表中位于第三周期,镁属于金属元素;故填:三;金属;
(2)16号元素是硫,其原子最外层有6个电子,在化学反应中易得到2个电子形成带两个单位负电荷的硫离子;故填:得到;S2-;
(3)元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,氟元素和氯元素化学性质相似的原因是它们的原子的最外层电子数相同.故填:氟或F;
(4)同一周期元素之间从左到右,各元素原子随原子序数的增加,最外层电子数从1到8依次递增;故填:最外层电子数增加.
(5)电荷数分别为11和17的元素为钠元素和氯元素,其中钠元素易失去一个电子,而形成阳离子,氯元素易得到一个电子而形成阴离子,所以它们组成的化合物为氯化钠,离子为:Na+,Cl-,故填:Na+、Cl-.
点评 本题难度不大,考查学生对原子结构示意图及其意义的理解,了解原子结构示意图的意义是正确解题的关键.

练习册系列答案
相关题目
10. 科学家最近在-100℃的低温下合成一种化合物X,此分子的模型如图,其中每个
科学家最近在-100℃的低温下合成一种化合物X,此分子的模型如图,其中每个  代表一个碳原子,每个
代表一个碳原子,每个  代表一个氢原子.下列说法中不正确的是( )
代表一个氢原子.下列说法中不正确的是( )
 科学家最近在-100℃的低温下合成一种化合物X,此分子的模型如图,其中每个
科学家最近在-100℃的低温下合成一种化合物X,此分子的模型如图,其中每个  代表一个碳原子,每个
代表一个碳原子,每个  代表一个氢原子.下列说法中不正确的是( )
代表一个氢原子.下列说法中不正确的是( )| A. | 该分子构成物质的化学式为C5H4 | |
| B. | 该分子中碳元素的质量分数是93.75% | |
| C. | 该分子中的氢原子与碳原子的个数比是4:5 | |
| D. | 该分子中含有两个氢分子 |
11.实验探究不仅可以锻炼同学们的动手能力,还可以帮助他们提升逻辑推理能力.下面两个探究实验,请根据信息回答相关问题.
探究一:化学课上,老师取出了一瓶课前准备好的无色无味的气体,如图1所示放在实验台上.同学们对该瓶气体产生浓厚的兴趣.
【提出问题】这到底是什么气体呢?
【猜想假设】①该瓶气体是氧气;②该瓶气体是二氧化碳;③该瓶气体可以是氮气.
【实验验证】
【交流反思】
小林认为,可用带火星的木条伸入集气瓶,若观察到不复燃现象,则猜想②正确.你认为他的说法否(填“是”或“否”)正确的,理由是不能支持燃烧的气体不只有二氧化碳.
探究二:实验是学习化学的一条重要途径,同学们想对铁丝在氧气中燃烧的现象进行探究.
【提出问题】铁丝在氧气中为什么会产生火星四射现象?
【查阅资料】
a.镁条、纯铁丝燃烧无火星四射现象;
b.含碳细铁丝燃烧时,其中的碳粒生成的二氧化碳气体在熔融液态物质中形成气泡,熔融液态物质因气泡炸裂引起“火星四射”现象.
【设计实验】
取纯铁丝的含碳量分别为0.1%、0.32%、0.52%、0.69%的铁丝(直径均为0.20mm)分别在氧气中进行实验(如图2).

ⅰ.铁丝的末端系一根火柴的作用给铁丝预热,引燃铁丝;
ⅱ.铁丝在氧气中燃烧的符号表达式3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
ⅲ.下表是实验中所记录的实验现象.
【得出结论】
铁丝燃烧产生火星四射现象和含碳量有关,就0.20mm铁丝而言,燃烧喷射火星情况与其含碳量的关系为含碳量越高,火星四射越剧烈.
【交流反思】
实验过程中用纯镁条实验的目的是对比.
探究总结:请结合已学知识以及上述两个探究实验,找出符合化学学习特点的选项ABC.
A.关注物质的性质;
B.关注物质的变化;
C.关注物质变化的过程以及对结果的解释和讨论.
探究一:化学课上,老师取出了一瓶课前准备好的无色无味的气体,如图1所示放在实验台上.同学们对该瓶气体产生浓厚的兴趣.
【提出问题】这到底是什么气体呢?
【猜想假设】①该瓶气体是氧气;②该瓶气体是二氧化碳;③该瓶气体可以是氮气.
【实验验证】
| 实验操作 | 现象 | 结论 |
| 用燃着的木条伸入集气瓶, | 木条燃烧更旺, | 猜想①正确; |
| 向集气瓶中滴入澄清石灰水,震荡, | 石灰水变浑浊, | 猜想②正确. |
小林认为,可用带火星的木条伸入集气瓶,若观察到不复燃现象,则猜想②正确.你认为他的说法否(填“是”或“否”)正确的,理由是不能支持燃烧的气体不只有二氧化碳.
探究二:实验是学习化学的一条重要途径,同学们想对铁丝在氧气中燃烧的现象进行探究.
【提出问题】铁丝在氧气中为什么会产生火星四射现象?
【查阅资料】
a.镁条、纯铁丝燃烧无火星四射现象;
b.含碳细铁丝燃烧时,其中的碳粒生成的二氧化碳气体在熔融液态物质中形成气泡,熔融液态物质因气泡炸裂引起“火星四射”现象.
【设计实验】
取纯铁丝的含碳量分别为0.1%、0.32%、0.52%、0.69%的铁丝(直径均为0.20mm)分别在氧气中进行实验(如图2).

ⅰ.铁丝的末端系一根火柴的作用给铁丝预热,引燃铁丝;
ⅱ.铁丝在氧气中燃烧的符号表达式3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
ⅲ.下表是实验中所记录的实验现象.
| 含碳量 | 纯镁条 | 纯铁丝 | 0.1% | 0.32% | 0.52% | 0.69% |
| 实验现象 | 发出耀眼白光,无火星四射现象 | 无火星四射现象,熔断 | 有短暂火星四射现象 | 火星四射现象明显 | 燃烧比0.32%剧烈,火星四射更明显 | 燃烧比0.52%剧烈,火星四射更明显 |
铁丝燃烧产生火星四射现象和含碳量有关,就0.20mm铁丝而言,燃烧喷射火星情况与其含碳量的关系为含碳量越高,火星四射越剧烈.
【交流反思】
实验过程中用纯镁条实验的目的是对比.
探究总结:请结合已学知识以及上述两个探究实验,找出符合化学学习特点的选项ABC.
A.关注物质的性质;
B.关注物质的变化;
C.关注物质变化的过程以及对结果的解释和讨论.
15.2015年10月,中国科学家屠呦呦凭借对青蒿素的研究成果获得了诺贝尔生理学或医学奖,青蒿素(化学式为:C15H22O5)是一种用于治疗疟疾的药物,曾拯救全球数百万生命,下列关于青蒿素的说法错误的是( )
| A. | C15H22O5表示青蒿素这种物质 | B. | 青蒿素是由C、H、O三种原子构成 | ||
| C. | 青蒿素是由C、H、O三种元素组成 | D. | 1个青蒿素分子中含有42个原子 |
 (1)如图所示容积为250mL的细颈瓶A中加水至虚线处,再滴几滴红墨水,一段时间后,A中的现象是液体变红色,说明分子是不断运动的.
(1)如图所示容积为250mL的细颈瓶A中加水至虚线处,再滴几滴红墨水,一段时间后,A中的现象是液体变红色,说明分子是不断运动的. 完成下列变化的化学方程式,并按要求填空.
完成下列变化的化学方程式,并按要求填空.